Diagnóstico de tos ferina en consultas de Pediatría de Atención Primaria
2 Facultativo Especialista de Área. Laboratorio de Microbiología. Hospital San Pedro. Logroño. La Rioja (España).
INTRODUCCIÓN
La tos ferina es una infección respiratoria aguda causada por bacterias del género Bordetella, cocobacilos gramnegativos. El agente causal más frecuente es la B. pertussis (Bp), cuyo principal factor de patogenicidad es la toxina pertussis (TP), muy importante en la inducción de la respuesta inmunológica. La TP es el componente fundamental de las vacunas acelulares frente a la enfermedad. Se cree que el único reservorio de Bp es el hombre.
Además de Bp, otras tres especies de Bordetella pueden causar enfermedad en el hombre: B. parapertussis (Bpp), B. holmesii y B. bronchiseptica. La enfermedad causada por B. parapertussis es similar a la tos ferina pero más leve, ya que B. parapertussis no produce la toxina pertussis. No es infrecuente encontrar coinfecciones de B. pertussis y B. parapertussis.
La enfermedad tiene un comienzo insidioso indistinguible de otras infecciones respiratorias leves (fase catarral), con tos irritativa que en de una a dos semanas progresa (fase paroxística) y puede acompañarse de un estridor inspiratorio característico. Los episodios de crisis de tos aumentan tanto en frecuencia como en gravedad y luego van cediendo, aunque la tos puede persistir hasta seis semanas más (fase de convalecencia).
La presentación clínica de la tos ferina varía con la edad y los antecedentes de vacunación. En menores de seis meses, el cuadro típico de estridor no suele desarrollarse y los paroxismos de tos pueden seguirse de periodos de apnea. En los adolescentes y adultos la enfermedad puede ser leve y no identificarse como tos ferina. Estos últimos precisamente suelen estar más en contacto con el grupo más vulnerable para la tos ferina grave, los lactantes pequeños, con cobertura vacunal ausente o parcial según la edad, por lo que la enfermedad es más frecuente en ellos. Además, este grupo presenta mayor riesgo de complicaciones y mayor mortalidad.
La infección se transmite por contacto directo con secreciones respiratorias o a través de gotas de saliva. Su periodo de incubación es de 7-10 días (con un intervalo máximo entre 6-20 días)1. Una persona con tos ferina es contagiosa desde el comienzo de la fase catarral hasta las dos primeras semanas después del inicio de la tos paroxística (aproximadamente 21 días) o hasta cinco días después de empezar con un tratamiento antibiótico eficaz2.
La susceptibilidad frente a B. pertussis es universal. Ni la infección natural por B. pertussis ni la vacunación confieren inmunidad duradera por lo que las reinfecciones son frecuentes. Según la Organización Mundial de la Salud (OMS) la tos ferina ocupa el quinto lugar como causa de muerte por enfermedad inmunoprevenible en menores de cinco años3.
Diferentes estudios seroepidemiológicos han demostrado la amplia circulación de B. pertussis en todo el mundo, independientemente de los calendarios y de las coberturas de vacunación. En España, como en otros países con políticas y tasas de coberturas vacunales similares, la tos ferina ha resurgido en los últimos años, aumentando en todos los grupos de edad, con una distribución por edades bimodal: en los lactantes menores de seis meses, que por su edad no han iniciado la primovacunación o no la han completado, y en los adolescentes y adultos por la disminución de su inmunidad, vacunal o natural4.
Entre las posibles causas de este aumento se señalan, además de la mejora en el acceso a técnicas de diagnóstico rápido que permiten una mejor notificación de la enfermedad, la evanescencia del efecto protector de la vacuna, un aumento de circulación de las cepas de Bp, cambios genéticos de las cepas circulantes y la menor efectividad de la vacuna acelular comparada con la de la vacuna de células enteras.
Este aumento de incidencia queda reflejado en el Informe sobre la situación de la tos ferina en España, 1998-2014, llevado a cabo por el Centro Nacional de Epidemiología, y se muestra en la tabla 15.
Tabla 1. Casos notificados, hospitalizaciones y mortalidad por tos ferina. España, 1998-2014. Mostrar/ocultar
No obstante, se cree que, en realidad, la incidencia de la enfermedad es superior a la que indican los datos de vigilancia epidemiológica, debido a la existencia de una infranotificación y un infradiagnóstico importantes6.
La importancia del diagnóstico reside en: tratar la infección para acortar síntomas y disminuir la transmisión de casos eliminando la bacteria de la nasofaringe de los afectados, la detección de los contactos, aumentar la notificación para conocer la incidencia real de la enfermedad y optimizar el uso de los antibióticos.
La mayor parte de los pacientes susceptibles están vacunados o parcialmente vacunados, siendo poco probable en ellos el desarrollo una tos ferina grave. Serán atendidos en su mayoría por sus pediatras de Atención Primaria (AP) especialmente en las fases iniciales de la enfermedad, que son por otro lado las de mayor contagiosidad.
¿CÓMO SE REALIZA EL DIAGNÓSTICO DE TOS FERINA?
Se considera (en base al Protocolo de vigilancia de tos ferina establecido por la Red Nacional de Vigilancia Epidemiológica):
- Caso sospechoso: persona que cumple los criterios clínicos.
- Caso probable: persona que cumple los criterios clínicos y tiene vínculo epidemiológico con un caso confirmado.
- Caso confirmado: persona que cumple los criterios clínicos y microbiológicos.
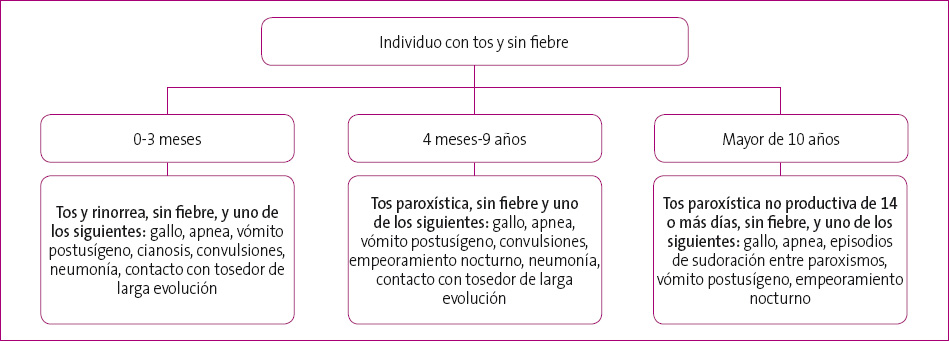
Los criterios clínicos de sospecha de tos ferina fueron actualizados por la Global Pertussis Initiative en 20127 y quedan resumidos en la Figura 1.
Figura 1. Criterios clínicos de sospecha de tos ferina8. Mostrar/ocultar
Los criterios microbiológicos incluyen al menos uno de los tres siguientes:
- Aislamiento de Bordetella pertussis en una muestra clínica (cultivo).
- Detección del ácido nucleico de Bordetella pertussis en una muestra clínica (técnicas de reacción en cadena de la polimerasa [PCR]).
- Respuesta de anticuerpos específicos frente a Bordetella pertussis (serología).
Criterio epidemiológico: contacto con un caso de tos ferina confirmado por laboratorio entre los 6 y 20 días antes del inicio de los síntomas.
En todos los pacientes que presenten criterios clínicos y/o epidemiológico de tos ferina debe realizarse confirmación microbiológica de la infección.
Se dispone de varios métodos de laboratorio para el diagnóstico de la tos ferina, destacando el cultivo, la serología y las técnicas de biología molecular.
El cultivo es el método de referencia; sin embargo, pese a que su especificidad es de casi el 100% (97,1%-99,7%)9, la sensibilidad es mucho menor y disminuye con el transcurso del tiempo, así como con el tratamiento antimicrobiano o la vacunación previa. El aislamiento de Bp en el cultivo requiere medios especiales, y su desarrollo puede llevar entre 7 y 14 días, por lo que los resultados podrían no estar disponibles a tiempo para tratar los casos agudos.
La serología, combinando dos extracciones en la fase aguda y en la fase de convalecencia, requiere de un intervalo de cuatro semanas entre la obtención de las muestras, por lo que no resulta de utilidad para el diagnóstico inmediato. A pesar de existir pruebas serológicas comercializadas, no están validadas clínicamente y no permiten diferenciar la infección reciente de la pasada o de la vacunación.
El empleo de técnicas de biología molecular en muestras respiratorias (aspirado o frotis nasofaríngeo) y en especial la PCR “en tiempo real”, se han ido generalizando en los últimos años. La mayor rapidez y sensibilidad de la técnica respecto al cultivo (hasta un 40% más)9 han llevado a OMS y a la CDC a incluirla en sus definiciones de “caso”, ya que ayudan en la toma precoz de decisiones terapéuticas y preventivas. Así mismo, su especificidad es teóricamente igual a la del cultivo siempre y cuando no existan problemas de contaminación9.
Para su realización, es necesario:
- Disponer de hisopos adecuados para la toma de frotis nasofaríngeos (FNF).
- Realizar una toma de muestra adecuada.
- Contar con la colaboración del Servicio de Microbiología de referencia en cada caso, en cuya cartera de servicios deben estar incluidas las técnicas de biología molecular para la detección de material genético de Bordetella pertussis/parapertussis.
¿CUÁLES SON LOS HISOPOS ADECUADOS PARA REALIZAR UN FNF?
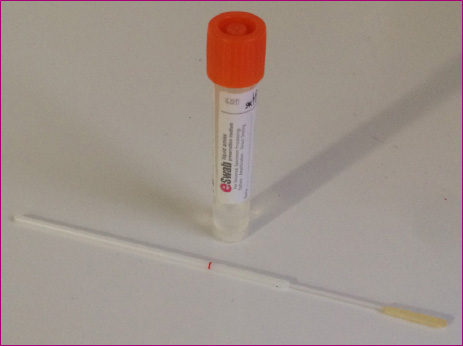
Deben ser finos y flexibles. Los hisopos de dacrón, rayón o nylon-flocked pueden utilizarse; sin embargo, los de algodón o alginato cálcico no son adecuados para la posterior realización de técnicas de PCR. Los hisopos deben ser transportados en medio de AMIES o medio de Stuart10 (Figura 2). En el caso de que la muestra solo se utilice para PCR, puede enviarse en medio transparente.
Figura 2. Hisopo y medio para FNF. Mostrar/ocultar
¿CÓMO SE REALIZA UN FROTIS NASOFARÍNGEO?
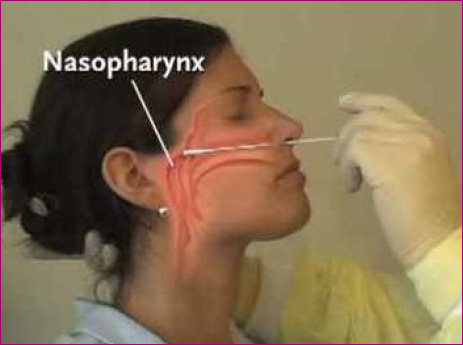
En la consulta de AP, la muestra debe ser tomada por el pediatra o enfermera de Pediatría (en cualquier caso, debe ser alguien instruido para su realización). Debe utilizar guantes para evitar contaminaciones y mascarilla para prevenir contagios. El paciente debe elevar ligeramente la cabeza (en posición de olfateo) y con la mano libre se eleva la pirámide nasal. El hisopo se introduce suavemente a través de la fosa nasal, paralelo al suelo de la misma, llegando a tocar la pared de la nasofaringe (figura 3). Una vez llegado a este punto, se debe ejercer un movimiento suave de rotación hacia ambos lados y se retira el hisopo.
Figura 3. Toma correcta de FNF. Mostrar/ocultar
La ECDC recomienda la visualización de un vídeo demostrativo (http://www.youtube.com/watch?v=d6d-y7SX_dY, del Instituto Pasteur)10.
El transporte de las muestras desde AP hasta los servicios de microbiología de referencia se puede llevar a cabo mediante la vía habitual utilizada en cada centro. En los casos en los que la recogida de muestras en los centros de AP no se realice a diario, la muestra debe conservarse entre 2-8 ºC hasta su transporte.
¿CÓMO SE REALIZA LA PCR A TIEMPO REAL PARA LA DETECCIÓN DE BP O BPP?
Esta técnica debe ser realizada en el Servicio de Microbiología de referencia en cada centro.
El proceso de detección del genoma del agente infeccioso se desarrolla de manera habitual en dos etapas:
- Extracción y purificación de los ácidos nucleicos de las muestras clínicas: en el mercado se encuentran disponibles gran cantidad de sistemas de purificación de ácidos nucleicos. Se debe realizar el procedimiento de purificación siguiendo las instrucciones del fabricante y partir del volumen de muestra recomendado.
- Reacción amplificación-detección: existen diversos métodos y equipos comerciales para la determinación de los ácidos nucleicos de Bordetella pertussis y parapertussis que han sido aprobados para diagnóstico in vitro. La mayoría de ellos están basados en la tecnología de PCR “a tiempo real”, la cual presenta múltiples ventajas con respecto a la técnica de PCR convencional, destacando especialmente la rapidez en la obtención de resultados, mayor sensibilidad10 y menor riesgo de contaminaciones (falsos positivos), pudiéndose utilizar incluso en pacientes que han recibido tratamiento antibiótico previo.
Algunos de los aparatos más utilizados según la ECCD son LightCycler®(Roche), Applied Biosystems, Stratagene, Rotor-GeneTM (Qiagen), SmartCycler (Cepheid) e ICycler (Bio-Rad)10.
Se realiza la amplificación de distintas secuencias de genes (dianas) según los kits utilizados, los cuales pueden estar presentes en varias especies de Bordetella, por lo que puede ser necesaria la realización de PCR secuenciales para conseguir identificar el microorganismo.
Se recomienda seguir los protocolos y recomendaciones de los fabricantes.
¿CUÁLES SON LAS LIMITACIONES DE LA PRUEBA?
- Los resultados del ensayo de detección de ADN de Bp/Bpp deben interpretarse en el contexto clínico de cada paciente.
- Dado que la sensibilidad de la técnica disminuye significativamente a partir de la tercera/cuarta semana desde el inicio de los síntomas, es importante que la toma de la muestra se realice en las fases iniciales (durante las tres primeras semanas desde el inicio de la tos).
- Es fundamental realizar una correcta toma de la muestra.
- La PCR es más sensible que el cultivo, pero puede dar resultados falsos positivos (dianas detectables en otras especies de Bordetella, contaminación por aislamientos o por amplificados de laboratorio) y falsos negativos (muestra o frotis inadecuados, recogida de la muestra a partir de la tercera semana del inicio de los síntomas, presencia de inhibidores en la muestra, daño del ADN bacteriano durante el procesamiento, infección por cepas con mutaciones/inserciones/supresiones en la diana, problemas técnicos)10.
- Hasta ahora no se ha estandarizado la técnica a utilizar y la sensibilidad y la especificad puede variar entre laboratorios, por lo que es importante conocer la técnica utilizada en cada centro y sus limitaciones.
CONCLUSIONES
- La tos ferina es una infección cuya incidencia ha aumentado en los últimos años, con importantes consecuencias de morbimortalidad especialmente en los pacientes menores de seis meses.
- Los cambios epidemiológicos y de estrategias vacunales acontecidos en los últimos años hacen que el pediatra deba estar especialmente vigilante en el diagnóstico de esta infección. El papel del pediatra de AP es fundamental, ya que suele ser el primero en sospechar la enfermedad.
- El tener a su disposición medios adecuados y rápidos para el diagnóstico es necesario para poder determinar la incidencia real de esta enfermedad, para la instauración de un tratamiento adecuado y la realización de estudios de contactos que corten la cadena de transmisión epidemiológica de la enfermedad, previniendo la aparición de nuevos casos.
- En este sentido la utilización de técnicas de PCR “a tiempo real” en muestras respiratorias (FNF) tomadas en la consulta de AP puede ser clave para conseguir estos objetivos.
BIBLIOGRAFÍA
LECTURAS RECOMENDADAS
- Lupiani Castellanos MP, Grande Tejada AM, Dapena Archiles M, Ares Álvarez J; Grupo de Patología Infecciosa de la Asociación Española de Pediatría de Atención Primaria. Tosferina ¿En qué punto nos encontramos? En: Asociación Española de Pediatría de Atención Primaria [en línea] [consultado el 01/12/2016]. Disponible en: http://www.aepap.org/sites/default/files/tosferina.pdf
- Centro Nacional de Epidemiología, Instituto de Salud Carlos III, Red Nacional de Vigilancia Epidemiológica. Tosferina. En: Protocolos de enfermedades de declaración obligatoria. Instituto de Salud Carlos III [en línea] [consultado el 01/12/2016]. Disponible en: http://www.isciii.es/ISCIII/es/contenidos/fd-servicios-cientifico-tecnicos/fd-vigilancias-alertas/PROTOCOLOS_RENAVE.pdf