Orientación, manejo y seguimiento de la enfermedad inflamatoria intestinal en la consulta de Atención Primaria
2 Hospital Universitario de Fuenlabrada. Fuenlabrada. Madrid (España).
3 Hospital Universitario Rey Juan Carlos. Móstoles. Madrid. (España).
PUNTOS CLAVE
- La enfermedad inflamatoria intestinal es una entidad en aumento, la enfermedad de Crohn es la forma más frecuente.
- Los síntomas digestivos son inespecíficos, como dolor abdominal y diarrea, pero se debe estar atento a los signos de alarma asociados y derivar de forma precoz al gastroenterólogo infantil puesto que el retraso diagnóstico determina una peor respuesta al tratamiento.
- No es desdeñable el porcentaje de manifestaciones extraintestinales que pueden asociarse, de las que la afectación osteoarticular es la más frecuente.
- El diagnóstico de sospecha se realiza ante la sospecha clínica, alteraciones de laboratorio y de las pruebas de imagen, así como en la exploración física. El diagnóstico definitivo se basará en la histología y endoscopia digestiva.
- En el diagnóstico diferencial deberemos descartar las infecciones gastrointestinales y la infección por Clostridium difficile.
- El tratamiento con nutrición enteral exclusiva es de elección en la enfermedad de Crohn y ha relegado los corticoides a un segundo plano. Los aminosalicilatos, inmunomoduladores y biológicos suelen utilizarse en el tratamiento de mantenimiento de la enfermedad.
- El seguimiento por el pediatra de Atención Primaria será primordial para promover hábitos de vida saludables, realizar valoraciones antropométricas seriadas, actualizar el calendario vacunal y reconocer los eventuales efectos secundarios de la medicación.
CASO CLÍNICO
Niño de 11 años que acude a control tras haber realizado 3 meses de tratamiento con ferroterapia oral por anemia ferropénica. En la consulta nos cuenta que en los últimos meses presenta dolor abdominal y diarrea con algo de moco, pero sin sangre, y que ambos le despiertan por la noche con urgencia defecatoria. Además, últimamente se queja de dolor en un tobillo que no le impide su actividad habitual, pero se le inflama de forma intermitente y tiene aftas orales frecuentes.
En su desarrollo ponderoestatural observamos un enlentecimiento de la velocidad de crecimiento y estancamiento ponderal en el último año.
En la analítica de control postratamiento con hierro encontramos anemia microcítica hipocroma, proteínas y albúmina bajas, proteína C reactiva (PCR) de 3 mg/dl y velocidad de sedimentación globular (VSG) de 80 mm/h. Solicitamos una calprotectina fecal con un valor de >3000 mg/kg.
EL PROBLEMA EN NUESTRO MEDIO
La incidencia de enfermedad inflamatoria intestinal (EII) en la edad pediátrica ha aumentado exponencialmente en los últimos 30 años en nuestro país, pasando de una incidencia de 0,97/100 000 habitantes hasta 2,8 por cada 100 000 habitantes actualmente según encontramos en los registros nacionales SPIRIT y EXPERIENCE (1985-2009)1,2 con un mayor aumento de la incidencia de la enfermedad de Crohn (EC) y colitis indeterminada (CI).
La edad media de diagnóstico pediátrico son los 12 años y solo un pequeño porcentaje de pacientes se diagnostican antes de los 5 años, siendo este grupo, junto con los pacientes con enfermedad ileal aislada en la EC, los que sufren un mayor retraso diagnóstico3. El retraso en el diagnóstico de la EII está relacionado con peor respuesta al tratamiento y una evolución hacia una mayor gravedad, factores que ya de por sí se asocian a la EII de diagnóstico en la edad pediátrica4.
La piedra angular para establecer la sospecha de una EII es el pediatra de Atención Primaria, dado que los síntomas clínicos más frecuentes son inespecíficos: dolor abdominal y diarrea. En manifestaciones clínicas como la rectorragia es más probable la consulta hospitalaria, si bien la mayoría de los pacientes con EII presentan una baja tasa de consulta en Urgencias y la sospecha diagnóstica viene hecha desde Atención Primaria.
Debemos estar alerta ante la asociación de síntomas digestivos con otros sistémicos como la astenia, pérdida de peso, febrícula, fisuras anales o artritis para sospechar precozmente el diagnóstico y realizar las pruebas complementarias pertinentes disponibles mientras se deriva el paciente al gastroenterólogo infantil, ya que el diagnóstico precoz es crucial para el buen manejo de una EII.
¿CUÁNDO SOSPECHAR UNA EII?
La EII produce con frecuencia manifestaciones sistémicas (fiebre, retraso del crecimiento, retraso puberal, astenia…) junto a manifestaciones digestivas y extradigestivas. Los síntomas y signos intestinales más frecuentes son el dolor abdominal, la diarrea y la malnutrición.
- Dolor abdominal: es más frecuente en la EC que en la colitis ulcerosa (CU). En casos de afectación del tracto digestivo superior, los síntomas pueden ser dolor posprandial, retroesternal o pirosis. Típicamente, los niños con EC ileocecal presentan malestar leve-moderado continuo a nivel de la fosa iliaca derecha a cuyo nivel en algunos casos podremos palpar una masa inflamatoria.
- Diarrea: es el síntoma cardinal de la EII del niño, y en la enfermedad activa casi siempre está presente5. El factor patogénico principal es la disminución de la superficie absortiva. Otros mecanismos implicados importantes son la inhibición de la absorción de agua y electrolitos por el proceso inflamatorio, así como el aumento de la secreción. El sobrecrecimiento bacteriano es frecuente en la EC, y contribuye a la malabsorción por varios mecanismos. La CU suele causar diarrea, casi siempre mucosanguinolenta. Son frecuentes las defecaciones nocturnas, así como la urgencia defecatoria y el tenesmo rectal. La diarrea de la EC depende del segmento afectado. Los síntomas son similares a la CU cuando participan el colon y el recto. En la enfermedad limitada al intestino delgado, las deposiciones son voluminosas y, generalmente, no se asocian a urgencia, tenesmo ni a sangre macroscópica.
- Desnutrición: es común en niños con EII y se relaciona con la actividad y la extensión de la enfermedad. Es más frecuente en la EC. La causa es multifactorial, pero en la mayoría de los niños, el factor fundamental es la reducción de la ingesta calórica por anorexia. Esta asociación se demuestra en la respuesta a la nutrición enteral en niños con EC. La maldigestión y malabsorción de nutrientes son un factor significativo en los niños con EC extensa y crónicamente activa.
- Retraso del crecimiento: es frecuente al diagnóstico, especialmente en EC. El primer factor afectado es el enlentecimiento de la velocidad de crecimiento. Esto puede progresar hasta una talla baja para la edad y retraso puberal. Hasta un 50% de pacientes con EC tienen un enlentecimiento de la velocidad del crecimiento antes de la aparición de síntomas digestivos6.
¿QUÉ TIPOS DE EII HAY Y QUÉ DIFERENCIAS EXISTEN ENTRE ELLAS?
La EII engloba a un grupo de entidades clínico-patológicas cuya característica principal es la inflamación crónica en diferentes localizaciones del tubo digestivo. Se trata de un proceso de naturaleza inmune con etiología multifactorial. La EII es una enfermedad crónica cuyo curso clínico alterna periodos de inactividad o remisión con periodos de actividad clínica de diversa intensidad, denominados brotes o recidivas.
Actualmente el concepto de EII engloba, según su patrón fenotípico, tres entidades: la enfermedad de Crohn, la colitis ulcerosa y la EII no clasificada (EIInC) o colitis indeterminada (CI)7 (Tabla 1).
Tabla 1. Características diferenciales de colitis ulcerosa y enfermedad de Crohn. Mostrar/ocultar
Enfermedad de Crohn
Puede afectar a cualquier segmento del tubo digestivo, desde la boca hasta el ano. Las localizaciones más frecuentes son el íleon terminal y el ciego. La afectación es transmural, pudiendo invadir desde la mucosa hasta la serosa intestinal, con lesiones que varían desde aftas superficiales a grandes úlceras profundas, con una extensión parcheada en la endoscopia. Histológicamente pueden aparecer granulomas no caseificantes, aunque no son patognomónicos. Las manifestaciones extraintestinales y sistémicas son frecuentes, siendo una de las más características las fístulas perianales.
La evolución presenta un curso crónico que, inicialmente presenta un patrón predominantemente inflamatorio, pudiendo evolucionar a fistulizante, estenosante o ambos.
Colitis ulcerosa
Presenta afectación exclusiva de la mucosa cólica de forma continua y difusa, con inicio habitualmente desde el recto, pudiendo extenderse de forma proximal hacia el ciego. El segmento más frecuentemente afectado es el recto, y la afectación perianal es excepcional. La forma más frecuente de presentación en niños es la pancolitis. Al no afectar a las capas inferiores a la mucosa, es excepcional la aparición de fístulas y estenosis.
Histológicamente, existe un patrón de afectación crónica limitado a la mucosa, con una lámina propia congestiva que asocia distorsión de las criptas o abscesos crípticos, sin observarse granulomas.
Síntomas como la diarrea, rectorragia, síntomas de urgencia defecatoria o tenesmo rectal conforman la clínica típica, y son reflejo de la afectación rectal, pudiendo asociar síntomas sistémicos si la afectación es extensa.
Enfermedad inflamatoria intestinal no clasificada
Aunque el término se utiliza de forma habitual, existe confusión sobre cuál es su significado real. En la práctica, consiste en una EII con afectación exclusiva de colon, cuyas características clínicas, endoscópicas e histológicas no permiten la diferenciación entre EC y CU.
¿QUÉ MANIFESTACIONES EXTRADIGESTIVAS SE PUEDEN ENCONTRAR?
La enfermedad inflamatoria intestinal puede considerarse una enfermedad sistémica, ya que a menudo asocia manifestaciones extraintestinales (MEI) que pueden afectar a casi todos los órganos y sistemas. No obstante, las MEI en niños están escasamente descritas. Se estima la presencia de, al menos, una MEI al diagnóstico en el 6% de los niños, y hasta en el 29% en un plazo de 15 años tras el mismo5,8 (Tabla 2).
Tabla 2. Manifestaciones extraintestinales en la enfermedad inflamatoria crónica. Mostrar/ocultar
Manifestaciones osteoarticulares
Son las más frecuentes. Constituyen un grupo heterogéneo de enfermedades asociadas con el HLA-B27. Los pacientes con EC y HLAB27+ desarrollan sacroileítis en el 100% de los casos. Entre ellas encontramos:
- Artropatía periférica: junto con la estomatitis aftosa, son las MEI más frecuentes en el diagnóstico. Puede ser pauciarticular (coincide con recaídas de EII y afecta a menos de 5 articulaciones) o poliarticular (evoluciona independientemente de los brotes).
- Artritis centrales: la sacroileítis puede detectarse en la mayoría de los pacientes, aunque es asintomática en la mayoría. No suele ir paralela a la actividad de la EII. La espondilitis anquilosante es más frecuente en pacientes con CU, y es independiente de la evolución.
Manifestaciones hepatobiliares
Cuando la afectación hepática tiene base inmunológica se incluye dentro de las MEI. La manifestación hepatobiliar más frecuente es la colangitis esclerosante primaria, y suele asociarse más con CU de afectación pancolónica. Es una enfermedad inflamatoria crónica del árbol biliar, que da lugar a fibrosis con cirrosis y fallo hepático. Su curso no parece relacionarse con el de la EII subyacente.
Manifestaciones dermatológicas
Manifestaciones cutáneas específicas: con las mismas características histopatológicas que la EII subyacente.
- Estomatitis aftosa: tiene una alta prevalencia en la población general. Se ha asociado con enfermedad perianal, pero no con otras MEI. Su tratamiento es sintomático.
- Manifestaciones perianales: incluyen abscesos y fístulas. Se producen por afectación local de la piel y de la mucosa subyacente. Cuando se observan en la exploración de un paciente no diagnosticado, deben ser un signo de alerta de EII.
Manifestaciones cutáneas reactivas: con mecanismos inmunológicos activados por antígenos compartidos.
- Eritema nodoso: se presenta como nódulos subcutáneos de color rojo-azulado, dolorosos y calientes, que se localizan en superficies de extensión de las extremidades. Relacionado con los brotes de enfermedad, su tratamiento es el de la EII subyacente.
- Pioderma gangrenoso: aparece como una pápula que evoluciona a una úlcera, con un anillo violáceo. La curación deja una cicatriz excavada clásica. Se relaciona con la actividad de la colitis.
Manifestaciones oculares
Su patogénesis se atribuye a una reacción de hipersensibilidad frente a antígenos colónicos.
- Epiescleritis: no se asocia a pérdida de visión y suele acompañar a la exacerbación de la enfermedad de base.
- Escleritis: el dolor ocular es intenso y puede ser grave. El tratamiento ha de ser agresivo para prevenir una significativa pérdida de visión.
- Uveítis: mucho menos frecuente, e independiente de la actividad de la EII subyacente. Sospechar si el paciente refiere cambios en la agudeza visual.
¿QUÉ HALLAZGOS SON CARACTERÍSTICOS EN LAS PRUEBAS COMPLEMENTARIAS?
La sospecha de EII se basa en una combinación de la historia clínica, exploración física, hallazgos de laboratorio y pruebas de imagen que conducen a la realización del diagnóstico definitivo por medio de la endoscopia digestiva alta y baja y la histología9 (Tabla 3).
Tabla 3. Pruebas complementarias que debemos solicitar ante la sospecha de enfermedad inflamatoria intestinal. Mostrar/ocultar
Hallazgos característicos de laboratorio
- Hemograma: anemia microcítica e hipocroma por pérdida crónica de sangre, leucocitosis y trombocitosis en brote.
- Proteínas y albúmina bajas por enteropatía pierde-proteínas, que reflejan severidad del brote.
- GOT, GPT y GGT elevadas en manifestaciones extraintestinales asociadas como patología hepatobiliar y colangitis esclerosante primaria.
- Ferropenia por las pérdidas de sangre, aunque es característico encontrar ferritina normal o elevada al ser un reactante de fase aguda, al igual que la transferrina. Deberemos tener en cuenta el perfil completo de hierro, siendo el parámetro más sensible el índice de saturación de transferrina disminuido.
- Serologías: anticuerpos anticitoplasma de neutrófilos (pANCA) y anti Saccharomyces cerevisiae (ASCA), apoyan al diagnóstico de CU y EC respectivamente
- Coprocultivo: ante la sospecha de EII será obligado descartar infecciones gastrointestinales, por lo que solicitaremos coprocultivo para bacterias (Salmonella, Shigella, Campylobacter y Yersinia), parásitos y toxina de Clostridium difficile. El hecho de encontrar un cultivo positivo no exime de la existencia de un brote de EII, ya que puede ser la causa desencadenante.
- Reactantes inflamatorios elevados en actividad aguda: VSG y PCR.
-
Calprotectina fecal: es una prueba útil, eficaz y no invasiva, dado que tiene una elevada sensibilidad para el diagnóstico de EII. Se puede alterar en otras patologías gastrointestinales que impliquen infección o inflamación intestinal, por ello la utilizaremos como indicador de inflamación con alto valor predictivo negativo10:
- Valores por debajo de 50-100 µg/g descartan con alta probabilidad la enfermedad en caso de sospecha clínica (valores validados para mayores de 4 años).
- Valores por encima de 200 µg/g harían necesaria la derivación hospitalaria para realización de más pruebas diagnósticas.
Pruebas de imagen
-
Ecografía: útil como herramienta de screening, no invasiva y con bajo coste. En manos expertas tiene un alto valor predictivo negativo. En caso de encontrar alteraciones se recomienda completar el estudio de imagen con pruebas más específicas. Los hallazgos que podemos encontrar son:
- Alteraciones murales: inflamación de la pared intestinal mostrada como pérdida de peristalsis y de la estratificación, así como alteraciones en el Doppler y en la ecogenicidad. En la EC encontraremos característicamente ileítis terminal.
- Alteraciones extramurales: adenopatías e hiperecogenicidad de la grasa mesentérica.
- Enterorresonancia magnética (ERM): se consigue una dilatación diagnóstica de asas intestinales con la realización de la RM tras la toma oral de sustancias no absorbibles, como polietilenglicol o sorbitoles. Es la prueba de imagen de elección al diagnóstico de EII dado que es inocua y detecta tanto la afectación del intestino delgado como los cambios inflamatorios de la pared intestinal y las complicaciones extraintestinales como fístulas, abscesos y estenosis.
- Vídeo cápsula endoscópica (VCE): será realizada en caso de no disponer de ERM o bien si sus resultados no son concluyentes a nivel del intestino delgado. Tiene mayor sensibilidad para detectar lesiones a nivel de la mucosa, si bien tiene muchas limitaciones que la hacen ocupar la segunda posición como prueba de imagen en la EII, que son: incapacidad para detectar complicaciones, imposibilidad de toma de biopsias, riesgo de retención e incapacidad de control del movimiento de la cápsula, alta incidencia de hallazgos incidentales y necesidad de ingesta de la cápsula Patency previo a su realización.
- Endoscopia: ante la sospecha de EII es obligado realizar una ilecolonoscopia con toma de múltiples biopsias de cada tramo (incluso si no se visualizan lesiones macroscópicas). Es necesario realizarla antes de iniciar el tratamiento, pues puede modificar los hallazgos. Será recomendable realizar también esofagogastroduodenoscopia con toma de biopsias en caso de sospecha de EII con clínica digestiva alta, por lo que generalmente de rutina se suelen programar de forma inicial y bajo el mismo acto anestésico la endoscopia digestiva alta y baja del paciente. La realización de la endoscopia se realizará con precaución ante brotes graves o sospecha de estenosis (importante para ello tener la ERM previa a su realización) y su única contraindicación absoluta es la presencia de megacolon tóxico, en cuyo caso habrá que esperar a su resolución para poder llevarla a cabo11.
¿CUÁNDO DERIVAR A LA CONSULTA DE ATENCIÓN ESPECIALIZADA?
En caso de presentar síntomas digestivos (dolor abdominal o diarrea prolongados) asociados a síntomas de alarma estará indicado realizar una derivación a la consulta de gastroenterología infantil12. Entre los signos y síntomas de alarma encontramos:
-
Historia clínica:
- Síntomas generales: pérdida de peso, astenia o fiebre.
- Fallo de crecimiento.
- Diarrea sanguinolenta sin causa identificada.
- Dolor abdominal que interfiere en las actividades de la vida diaria.
- Dolor abdominal o diarrea que no respeta el sueño.
- Urgencia defecatoria o tenesmo rectal.
-
Exploración física:
- Dolor abdominal persistente localizado en fosa iliaca derecha.
- Palidez cutánea.
- Colgajos anales (tags).
- Inflamación o abscesos perianales.
- Fisuras profundas o persistentes.
- Fístulas anales.
-
Analítica y ecografía abdominal: sospecha de organicidad según lo indicado en el apartado pruebas complementarias:
- Anemia, leucocitosis, trombocitosis.
- Proteínas y albúmina bajas.
- Ferropenia e IST bajo.
- Transaminasas elevadas.
- Elevación PCR y VSG.
- Elevación calprotectina fecal.
¿QUÉ ENTIDADES SE DEBEN PLANTEAR EN EL DIAGNÓSTICO DIFERENCIAL?
La EII pediátrica puede presentarse con sintomatología similar a la que presentan otras patologías gastrointestinales más frecuentes en la edad infantil, por lo que, en ausencia de datos de alarma, debemos pensar en ellas antes6,13.
- Infecciones intestinales: en función del agente implicado, puede variar la sintomatología y el tramo intestinal afecto. Habrá que descartarlas a través del coprocultivo, estudio de parásitos y detección de la toxina de C. difficile.
- Enfermedad celíaca: los marcadores serológicos positivos y los hallazgos endoscópicos confirmarán el diagnóstico. No obstante, ambas patologías pueden coexistir.
- Alergia alimentaria: los cuadros no IgE mediados pueden presentarse como una enteropatía, enterocolitis o proctocolitis, que suele evolucionar favorablemente con la exclusión de las proteínas implicadas en la dieta, lo que contrasta con la evolución tórpida de la EII.
- Trastornos eosinofílicos primarios: en este grupo de patologías se evidencia un aumento de eosinófilos en la mucosa intestinal y suelen responder bien a las dietas de exclusión. No obstante, en algunos casos no hay antecedente de alergia ni respuesta dietética y la sintomatología se controla bien con esteroides.
- Trastornos funcionales: incluyen afecciones que cursan con síntomas gastrointestinales recurrentes con componente afectivo-emocional asociado. La ausencia de síntomas de alarma, de complicaciones y de alteraciones en las pruebas complementarias sugieren este diagnóstico.
- Otras: si el síntoma predominante es la rectorragia habrá que descartar otras causas como los pólipos, hemorroides, estreñimiento, fisura anal, divertículo de Meckel, púrpura…
¿CUÁL ES EL TRATAMIENTO?
En los últimos años, el objetivo terapéutico de la enfermedad inflamatoria intestinal ha sido no solo alcanzar la remisión clínica, sino lograr la curación mucosa, ya que esto se relaciona con una mejor evolución de la enfermedad y una menor necesidad de tratamiento quirúrgico.
La elección del tratamiento se hará en función de diversos factores, entre los que cabe destacar: gravedad del brote, extensión, fenotipo, tratamientos previos, estado nutricional, edad del paciente y experiencia del equipo médico14.
- Nutrición enteral exclusiva (NEE): consiste en la utilización de una fórmula polimérica por vía oral durante 6-8 semanas como alimentación exclusiva. Se considera el tratamiento de primera línea en la EC leve-moderada, ya que es eficaz para alcanzar la remisión clínica y curación de la mucosa sin presentar efectos adversos importantes, a diferencia de los corticoides. Además, tiene efecto positivo en el crecimiento lineal y la ventaja de permitir ajustar las inmunizaciones antes de recibir inmunomoduladores o agentes biológicos.
- Aminosalicilatos: no se ha demostrado su eficacia ni en la inducción de la remisión ni como tratamiento de mantenimiento en la EC pediátrica. Se recomiendan como tratamiento de primera línea en la inducción de la remisión en brotes leves o moderados de CU.
- Corticoesteroides: se emplean para el control rápido del brote en caso de falta de respuesta a otros tratamientos, pero no logran la remisión histológica. Además, tienen múltiples efectos adversos entre los que cabe destacar la repercusión en el crecimiento lineal y la disminución de la densidad mineral ósea. Por ello, lo ideal es utilizarlos el menor tiempo posible, nunca como tratamiento de mantenimiento, hacer descenso gradual de dosis y suplementar con calcio y vitamina D durante su utilización.
- Inmunomoduladores: los agentes tiopurínicos, como la azatioprina (AZA) y su metabolito activo, la 6-mercaptopurina (6-MP), son eficaces como tratamiento de mantenimiento en la EC y la CU. El inicio de su efecto terapéutico no es inmediato, precisando al menos 3 meses. Este tiempo de respuesta obliga a iniciarlos a la vez que el tratamiento de inducción a la remisión con esteroides, NEE o fármacos biológicos. En cuanto al metotrexato, existen pocos estudios en población pediátrica, pero cuando la AZA y 6-MP no se toleran o son ineficaces, puede ser una alternativa. Tiene la ventaja de que el inicio de acción es más temprano, en torno a las 4 semanas.
- Inhibidores de la calcineurina: la experiencia del uso de tacrolimus o ciclosporina en la EC es muy escasa. La evidencia actual, aunque de pobre calidad, apoya el uso del tacrolimus en la EC del adulto.
- Terapia biológica: el infliximab (IFX) es un inhibidor del factor de necrosis tumoral (anti-TNFα) de administración intravenosa, útil en la inducción y mantenimiento de la remisión de la EC pediátrica moderada-grave. El adalimumab subcutáneo es otro anti-TNFα cuya indicación habitual en la práctica clínica hasta hace poco, eran los pacientes que habían perdido respuesta a IFX o eran intolerantes a este. Sin embargo, los datos disponibles avalan su eficacia y seguridad en la inducción de la remisión en la EC y la tasa de respuesta es mayor en aquellos que no han sido tratados previamente con otros biológicos. En los últimos años se han desarrollado otros fármacos biológicos como el vedolizumab, ustekinumab, etc.
-
Otros tratamientos utilizados:
- Antibióticos, como ciprofloxacino y metronidazol, cuyo uso debe reservarse para el tratamiento de las complicaciones sépticas o de la enfermedad perianal.
- Probióticos: las guías concluyen que en la EC no existe evidencia suficiente para recomendar su uso. Su principal indicación es en la reservoritis recurrente y los mejores resultados se han obtenido con VSL#3.
- Cirugía: las principales indicaciones de colectomía en la edad pediátrica son casos refractarios a tratamiento médico que asocian desnutrición y el retraso en el crecimiento, seguida de la obstrucción intestinal secundaria a un patrón estenosante y hemorragia intensa incontrolable. La enfermedad perianal también puede ser subsidiaria de cirugía y precisa fistulectomía si no responde a tratamiento médico.
¿QUÉ CUIDADOS HAY QUE TENER EN EL SEGUIMIENTO DE LOS PACIENTES DIAGNOSTICADOS DE EII, EN LA CONSULTA DE AP?
La gravedad de esta patología hace necesario un abordaje multidisciplinar en el que, además del seguimiento estrecho por el gastroenterólogo pediátrico, estén implicados otros profesionales sanitarios. Sin duda el pediatra de Atención Primaria tendrá un papel fundamental en el seguimiento de estos pacientes, con las siguientes misiones:
- Insistir en la importancia de una alimentación sana y equilibrada, recomendando evitar alimentos procesados o excesivamente condimentados, y realizando encuesta dietética de 3 o 5 días con el fin de detectar hábitos inadecuados. Además, vigilará la aparición de deficiencias nutricionales: vitamina B12, ácido fólico, calcio, vitamina D y hierro fundamentalmente, suplementando en los casos que sea necesario15.
- Detectar necesidad de apoyo psicológico en pacientes con afectación del desarrollo en las actividades de la vida diaria por la enfermedad que puedan ocasionar depresión, ausencia escolar, trastorno en la interacción social y familiar del paciente o trastornos de sueño16.
-
Valorar la antropometría (peso, talla, índice de masa corporal [IMC] y desarrollo puberal) cada 4 meses si el paciente está en remisión o antes si mantiene actividad. Se consideran datos de alarma una velocidad de crecimiento inferior a 4 cm al año o un IMC
17,18. - Determinar niveles de vitamina D al menos una vez al año, ya que hasta un 30% de los niños con EII tienen osteopenia. En este sentido se debe recomendar una ingesta adecuada de calcio y vitamina D, y realizar ejercicio físico17.
-
Identificar los efectos secundarios de los fármacos14 (Tabla 4):
Tabla 4. Efectos secundarios de fármacos y actitud a tomar. Mostrar/ocultar
- Nutrición enteral: casos aislados de hipertransaminasemia.
- Aminosalicilatos (5-ASA): infertilidad reversible en el varón en tratamiento con sulfasalazina. En el caso de la mesalazina aparecen en <2% y suelen ser inespecíficos (cefalea, náuseas, vómitos, dolor abdominal…).
- Corticoides: disminución de la densidad mineral ósea y riesgo aumentado de infecciones, principalmente.
- Inmunomoduladores: las tiopurinas pueden producir supresión de la médula ósea, pancreatitis, hepatotoxicidad, fiebre recurrente e infecciones, por lo que se debe realizar analítica que incluya hemograma, perfil hepatorrenal y lipasa cada 3 meses. Además, producen fotosensibilidad, por lo que se insistirá en el uso de protección solar alta con pantalla total.
- En las adolescentes en tratamiento con metotrexato, se insistirá en la contraindicación en el embarazo.
- Biológicos: ocasionan mayor predisposición a padecer infecciones o empeoran las existentes. Por ello, antes de iniciar el tratamiento se debe hacer despistaje de tuberculosis, virus de la hepatitis B y C, virus de la inmunodeficiencia humana, virus varicela-zóster, virus de Epstein-Barr.
- Se han relacionado con un riesgo aumentado de linfoma no Hodgkin o linfoma hepatoesplénico de células T, fundamentalmente en aquellos en los que se asocia azatioprina.
-
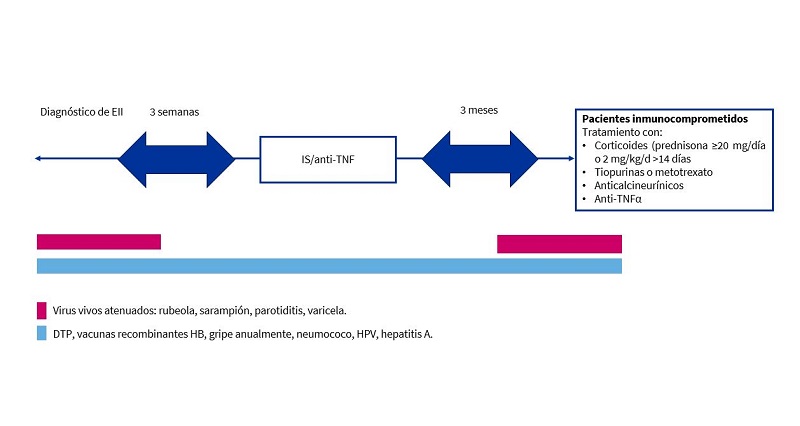
Comprobar el estado vacunal del paciente y tener en cuenta que las vacunas de virus vivos atenuados deberán administrarse al menos 3 semanas antes de iniciar la terapia inmunosupresora, y en el caso de que ya se haya instaurado, estarán contraindicadas hasta 3 meses después de concluirla. Se deberá vacunar frente al neumococo y anualmente frente a la gripe13,19 (Figura 1).
Figura 1. Planificación vacunal en paciente inmucomprometido con EII. Mostrar/ocultar
RESOLUCIÓN DEL CASO CLÍNICO
Ante la clínica referida y los hallazgos de laboratorio, se deriva el paciente a la consulta de Gastroenterología, donde se realiza una endoscopia digestiva alta y baja objetivando úlceras e inflamación en íleon, colon ascendente y recto. En la histología nos informan presencia de granulomas y fibrosis con afectación transmural. Se completa el estudio con una ERM que descarta la existencia de fístulas. Con todo ello se diagnostica de EII compatible con enfermedad de Crohn y se inicia tratamiento con NEE exclusiva durante 8 semanas y azatioprina como tratamiento de mantenimiento con normalización de reactantes y mejoría de la clínica, así como recuperación ponderoestatural.
BIBLIOGRAFÍA
- Martín-de-Carpi J, Rodríguez A, Ramos E, Jiménez S, Martínez-Gómez MJ, Medina E, et al. The complete picture of changing pediatric inflammatory bowel disease incidence in Spain in 25 years (1985-2009): the EXPERIENCE registry. J Crohns Colitis. 2014;8:763-9.
- Martín-de-Carpi J, Rodríguez A, Ramos E, Jiménez S, Martínez-Gómez MJ, Medina E, et al. Increasing incidence of pediatric inflammatory bowel disease in Spain (1996-2009): the SPIRIT Registry. Inflamm Bowel Dis. 2013;19:73-80.
- Arcos-Machancoses JV, Donat-Aliaga E, Polo-Miquel B, Masip-Simó E, Ribes-Koninckx C, Pereda-Pérez A. Retraso diagnóstico en la enfermedad inflamatoria intestinal pediátrica. Descripción y estudio de los factores de riesgo. An Pediatr (Barc). 2015;82:247-54.
- Timmer A, Behrens R, Buderus S, Findeisen A, Hauer A, Keller K-M, et al. Childhood onset inflammatory bowel disease: predictors of delayed diagnosis from the CEDATA German-language pediatric inflammatory bowel disease registry. J Pediatr. 2011;158:467-473.e2.
- Argüelles Martín F, García Novo MD, Pavón Relinchón P, Román Riechmann E, Silva García G, Sojo Aguirre A. Tratado de gastroenterología, hepatología y nutrición pediátrica aplicada de la SEGHNP. Madrid: Ergon; 2011. p. 325-340.
- Sánchez Sánchez C, Álvarez Calatayud G, Tolín Hernani MM. Manual práctico de enfermedad inflamatoria intestinal pediátrica. Madrid: Ergon; 2015. p. 45-51.
- Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica. Tratamiento en gastroenterología, hepatología y nutrición pediátrica. Madrid: Ergon; 2016. 235-251.
- Romeo Donlo M, Pizarro Pizarro I. Enfermedad inflamatoria intestinal: importancia del diagnóstico precoz. Rev Pediatr Aten Primaria. 2014; 16:49-53.
- Levine A, Koletzko S, Turner D, Escher JC, Cucchiara S, de Ridder L, et al. ESPGHAN revised porto criteria for the diagnosis of inflammatory bowel disease in children and adolescents. J Pediatr Gastroenterol Nutr. 2014;58:795-806.
- Cenarro Guerrero T. Utilidad de la determinación de calprotectina en el niño. Form Act Pediatr Aten Prim. 2017;10:143-4.
- Martínez Gómez MJ. Enfermedad inflamatoria intestinal pediátrica. Pediatr Integral. 2015;19:119-26.
- Grupo Gastrosur-Oeste. Protocolo de hemorragia digestiva baja. En: Asociación Madrileña de Pediatría de Atención Primaria [en línea] [consultado el 16/09/2019]. Disponible en: http://www.ampap.es/wp-content/uploads/2014/05/Hemorragia_digestiva_baja_2011.pdf
- Ricart E, Martín de Carpi J. Enfermedad inflamatoria intestinal en la edad pediátrica. Barcelona: Marge Médica Books; 2013. p. 67-73.
- Sánchez Sánchez C, Marín Jiménez I, Tolin Hernani MM. Enfermedad inflamatoria intestinal en Pediatría. Madrid: Ergon; 2013. p. 171-182.
- Rufo PA. Important health maintenance issues for children and adolescents with inflammatory bowel disease. En: UpToDate [en línea] [consultado el 16/09/2019]. Disponible en: https://www.uptodate.com/contents/important-health-maintenance-issues-for-children-and-adolescents-with-inflammatory-bowel-disease
- Romero MLC I Ros Arnal, T Cenarro Guerrero, R García. Protocolo de actuación en Atención Primaria en la enfermedad inflamatoria intestinal en la edad pediátrica. Acta Pediatr Esp. 2019;77:56-61.
- Zitomersky N, Bousvaros A. Overview of the management of Crohn disease in children and adolescents. En: UpToDate [en línea] [consultado el 16/09/2019]. Disponible en: https://www.uptodate.com/contents/overview-of-the-management-of-crohn-disease-in-children-and-adolescents
- Teitelbaum JE. Growth failure and poor weight gain in children with inflammatory bowel disease. En: UpToDate [en línea] [consultado el 16/09/2019]. Disponible en: https://www.uptodate.com/contents/growth-failure-and-poor-weight-gain-in-children-with-inflammatory-bowel-disease
- Veereman-Wauters G, de Ridder L, Veres G, Kolacek S, Fell J, Malmborg P, et al. Risk of infection and prevention in pediatric patients with IBD: ESPGHAN IBD Porto Group Commentary. J Pediatr Gastroenterol Nutr. 2012;54:830-7.