Proctocolitis hemorrágica: diagnóstico diferencial y orientación clínica en la consulta de Atención Primaria
2 Hospital Universitario Rey Juan Carlos. Móstoles. Madrid. (España).
3 Hospital Universitario Rey Juan Carlos. Móstoles. Madrid. (España).
PUNTOS CLAVE
- Para realizar el diagnóstico diferencial de una hemorragia digestiva se deberá tener en cuenta las características y la cuantía del sangrado, así como la edad del paciente.
- No existen pruebas complementarias específicas para el diagnóstico de la alergia a la proteína de la leche de vaca (APLV) no IgE mediada. Solo se realizará prick test o IgE específica en casos dudosos o bien antes de la adquisición de tolerancia en casos con clínica inmediata, FPIES o síntomas de marcha atópica por la probabilidad de sensibilización IgE tras la exclusión prolongada.
- El diagnóstico definitivo de APLV no IgE mediada en cualquiera de sus formas se basará en la prueba de exclusión-provocación.
- No siempre es necesario retirar las PLV en la dieta materna. Se mantendrán cuando la clínica esté claramente relacionada temporalmente con la introducción de leche adaptada.
- Las fórmulas elegidas para el tratamiento de una APLV no IgE mediada serán fórmulas extensamente hidrolizadas y, en casos seleccionados, fórmulas elementales de arroz o soja. Las fórmulas parcialmente hidrolizadas, bebidas vegetales o derivadas de otros mamíferos no están indicadas en ningún caso.
- La prueba de adquisición de tolerancia se realizará en la mayoría de los casos en domicilio y de forma progresiva, tras 6-12 meses de exclusión.
- No es preciso adaptar el calendario vacunal ni prescribir adrenalina autoinyectable en ninguno de los casos de APLV no IgE mediada.
- No existe evidencia científica de que ninguna intervención alimentaria en el niño o la madre prevengan el desarrollo de esta patología.
CASO CLÍNICO
Lactante de 4 meses, sin antecedentes perinatales de interés, al que traen a consulta por haber comenzado a presentar deposiciones con hebras escasas de sangre y moco en cantidad progresivamente mayor desde hace 1 semana.
En la exploración física, el estado general es bueno, no presenta signos de deshidratación ni palidez, está contento y activo y su ganancia ponderal es adecuada y mantenida en percentil 15 desde el nacimiento. Como único hallazgo en la exploración presenta leve eritema perianal.
En la anamnesis destaca que mantiene lactancia materna hasta la fecha, pero hace 2 semanas ha comenzado con suplementos de fórmula adaptada coincidiendo con la incorporación de la madre al trabajo.
EL PROBLEMA EN NUESTRO MEDIO
El hecho de encontrar una hematoquecia con cantidad de sangre escasa en un lactante menor de 6 meses, coincidente con la introducción de fórmula adaptada y sin signos de alarma, nos debe hacer pensar en primer lugar en una proctocolitis alérgica como forma de manifestación de una APLV.
La APLV es la alergia alimentaria más frecuente en los niños menores de 1 año. Dentro de la alergia no IgE mediada, la proctocolitis alérgica es una de las manifestaciones más frecuentemente observada, siendo el 60% de los niños sensibilizados incluso únicamente a través de la lactancia materna (LM) y las proteínas de leche de vaca (PLV) el principal alérgeno implicado.
Existe disparidad en la estimación de la prevalencia de esta entidad debido al uso de distintos criterios diagnósticos (incluidos criterios médicos subjetivos), así como las diferencias existentes según el país, etnia, estado socioeconómico y raza, aunque se ha observado mayor prevalencia en países industrializados y en población infantil. En Europa se estima una prevalencia de alergia alimentaria global del 6% (5,7-6,4%), con una prevalencia para APLV de 0,54% (0,41- 0,70%)1. En algunos estudios españoles refieren una prevalencia de hasta el 3% en menores de 1 año que desciende hasta menos del 1% en mayores de 6 años2.
ORIENTACIÓN CLÍNICA EN LA CONSULTA DE ATENCIÓN PRIMARIA
- Diagnóstico diferencial de hemorragia digestiva baja.
- ¿Cuándo sospechar y cómo diagnosticar una APLV no IgE mediada?
- ¿Es necesario retirar las PLV al niño y a la madre? ¿Qué fórmulas estarán indicadas en el tratamiento en caso de no mantener LM?
- ¿Dónde y cómo debe realizarse la prueba de adquisición de tolerancia?
- ¿Es necesario algún cambio en el calendario vacunal o prescribir adrenalina autoinyectable en pacientes con APLV no IgE mediada?
- ¿Se puede prevenir el desarrollo de la APLV no IgE mediada?
Diagnóstico diferencial de la hemorragia digestiva baja
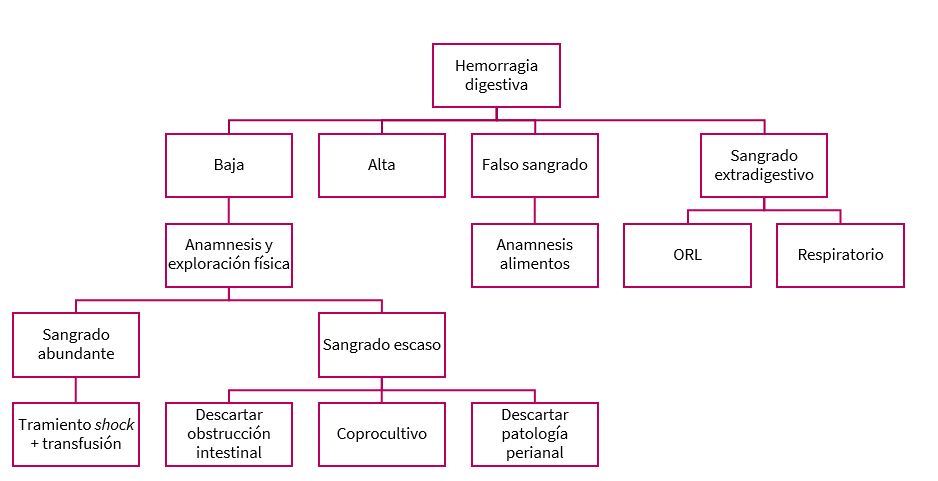
Debemos tener en cuenta varios factores para hacer el diagnóstico diferencial en casos de sangrado digestivo, como son la edad, características del sangrado y cuantía de este, además de otros síntomas acompañantes3 (Figura 1).
Figura 1. Diagnóstico diferencial de hemorragia digestiva baja. Mostrar/ocultar
De forma práctica realizaremos el diagnóstico diferencial en 2 pasos.
En primer lugar, tendremos en cuenta las características del sangrado y podremos clasificar entre:
- Hemorragia digestiva alta (HDA): aquella que ocurre por encima del ángulo de Treitz. Se expresará generalmente en forma de melenas (heces negras, alquitranadas y pegajosas).
- Hemorragia digestiva baja (HDB): aquella que ocurre por debajo del ángulo de Treitz. Se expresará generalmente en forma de hematoquecia o rectorragia (sangre roja, fresca y brillante).
- Falso sangrado: generado por alimentos con colorantes naturales que podrán teñir las heces sin ser realmente causas de sangrado (por ejemplo, espinacas, tomate, gelatinas o chocolate negro).
- Sangre de origen extradigestivo, siendo los casos más frecuentes, la sangre deglutida en los lactantes (por grietas en el pezón), de origen otorrinolaringológico (ORL) o respiratorio.
En segundo lugar, una vez que hemos identificado que se trata de una verdadera HDB tendremos que realizar la anamnesis y exploración física que nos permita valorar la magnitud del sangrado:
- Si la cuantía es abundante con inestabilidad hemodinámica: remitir al hospital para tratamiento del shock, así como valorar transfusión y pruebas urgentes.
-
Si la cuantía es escasa y no hay patología rectal apreciable en la exploración física, debemos descartar signos de obstrucción intestinal, utilizando en caso necesario radiografía de abdomen o ecografía; si no hay datos de obstrucción valoraremos otras etiologías:
- Infecciosas.
- Proctocolitis alérgica.
- Descartar antecedentes familiares de poliposis familiar o enfermedad inflamatoria intestinal.
- Descartar procesos ORL o respiratorios.
- Descartar ingesta de alimentos que tiñen heces.
En tercer lugar, también podremos orientar el origen del sangrado en función de la edad también según se recoge en la Tabla 14.
Tabla 1. Causas de hemorragia digestiva baja en función de la edad. Mostrar/ocultar
¿Cuándo sospechar y cómo diagnosticar una APLV no IgE mediada?
La forma principal de presentación de esta entidad es gastrointestinal y se puede clasificar en 3 grupos:
- Proctocolitis alérgica.
- Enteropatía alérgica.
- FPIES.
El diagnóstico se realizará ante sospecha clínica y por tanto la realización de la prueba de exclusión-provocación (PEP) será la única forma de confirmar el diagnóstico.
La presentación de un sangrado escaso en un lactante con ganancia ponderal adecuada, sin otros síntomas asociados y alimentación sin rechazo orienta hacia una proctocolitis alérgica.
La enteropatía alérgica se manifiesta como una combinación variable de diarrea, vómitos, irritabilidad, hiporexia, distensión abdominal y fallo de medro.
Por último, la FPIES o síndrome de enterocolitis inducido por proteínas se manifiesta en su forma aguda como vómitos entre 1-4 horas posingesta, generalmente violentos y que conducen a un decaimiento que puede llegar a situación shock-like. Entre episodios, el paciente se encuentra asintomático y con ganancia ponderal adecuada.
Ni las pruebas cutáneas (PC) ni las IgE específicas, ni ninguna otra prueba complementaria tendrán ningún papel confirmatorio en el diagnóstico. En el caso de las PC/IgE, su resultado será negativo en la gran mayoría de los pacientes, mientras que la analítica de sangre y la endoscopia digestiva mostrarán hallazgos inespecíficos.
La PEP se realizará en 3 pasos:
- Exclusión. Ante la sospecha clínica se retirará el alimento implicado, en este caso las proteínas de leche de vaca (presentes en la leche y derivados).
- Mejoría. Tras la retirada, el niño experimentará una mejoría clínica que se advertirá desde los primeros días en los casos de las FPIES, y en 2-4 semanas en el resto de entidades.
- Provocación. Una vez alcanzada la mejoría completa se reintroduce el alimento. Si se reproducen los síntomas iniciales se considera la prueba positiva y se confirma el diagnóstico de APLV, por lo que se retira de nuevo el alimento durante al menos 3-6 meses.
La realización de la provocación, ya sea hospitalaria o domiciliaria, se llevará a cabo progresivamente siguiendo las mismas recomendaciones que la prueba de adquisición de tolerancia y se vigilará la aparición de síntomas entre 2-4 semanas tras la reintroducción del alimento5.
¿Es necesario retirar las PLV al niño y a la madre? ¿Qué fórmulas estarán indicadas en el tratamiento en caso de no mantener LM?
El tratamiento indicado se decidirá en función de la alimentación del niño, donde encontraremos distintos escenarios (Tabla 2):
Tabla 2. Tipos de fórmulas indicadas según el momento de aparición de la APLV. Mostrar/ocultar
- Niño alimentado con LM exclusiva que se ha sensibilizado a través de ella (característico en las proctocolitis alérgicas). En este caso se retirarán las PLV de la dieta materna en primer lugar y en casos seleccionados muy graves (anemia o hipoproteinemia importantes) se podrá valorar una dieta elemental en el lactante mientras la madre se extrae la leche y el lactante se estabiliza. Si tras la exclusión de PLV persistieran los síntomas, se planteará la exclusión de otros alimentos alergénicos, siendo la soja y el huevo los siguientes alimentos implicados en frecuencia, aunque puede ser un verdadero reto diagnóstico encontrar el alimento implicado en caso de que no sea ninguno de los anteriores. En todas las madres que se retiren las PLV se recomendará suplementación de calcio (1 g/día) y vitamina D (400 UI/día)6.
- Niño alimentado con LM y que comienza con síntomas tras introducción de LA (ya sea lactancia mixta o artificial exclusiva). En este caso no será necesario modificar la dieta materna puesto que no hubo síntomas durante el tiempo inicial que se alimentó con ella, y se comenzará alimentación con fórmula extensamente hidrolizada manteniendo LM de forma normal.
Según los consensos de todas las sociedades las fórmulas de elección para el tratamiento en primer lugar de una APLV no IgE mediada leve-moderada serán las fórmulas extensamente hidrolizadas (FEH) de caseína o seroproteínas que son las que contienen oligopéptidos menores de 3000 Da (la mayoría por debajo de 1000 Da)5.
Existen otras opciones terapéuticas que hay que valorar, como:
- Fórmulas elementales: compuestas por aminoácidos libres, su indicación se reservará para los casos graves con fallo de medro, hipoproteinemia o anemia graves o en los que persistan los síntomas tras haber introducido una FEH. Existe controversia entre las diferentes sociedades, sobre la recomendación de utilizarlas en primer lugar para casos de FPIES, alergias alimentarias múltiples, lactantes con eccema grave sensibilizados con LM exclusiva o inestabilidad hemodinámica por sangrado rectal7.
- Fórmulas de arroz: se pueden utilizar desde el nacimiento en lactantes que no respondan a las FEH o no acepten el sabor de estas o de las fórmulas elementales.
- Fórmulas de soja: se pueden utilizar en los mismos casos que las de arroz, pero a partir de los 6 meses, ya que por debajo de esta edad existe mayor posibilidad de reacción cruzada a soja en estos niños.
Las fórmulas que no serán válidas para utilizar en ningún caso para una APLV no IgE mediada serán:
- Fórmulas parcialmente hidrolizadas (FPH): mantienen una alta capacidad antigénica debido a que no se afecta la secuencia peptídica (solo se altera la estructura) y por tanto no están indicadas en estos pacientes.
- Fórmulas de otros mamíferos como cabra u oveja, ya que por la similitud antigénica de sus proteínas con la leche de vaca habrá una alta tasa de reacciones cruzadas y por tanto no están indicadas.
- Bebidas vegetales: por su baja calidad nutricional y escaso contenido proteico no se indican como bebida principal por debajo de los 2 años; por encima de esa edad y dado que se extingue la financiación de las FEH por parte del Estado, se podrán utilizar dentro de una alimentación variada y completa, siendo siempre preferibles las fórmulas de soja y arroz en polvo.
En cuanto al resto de alimentación, a partir del momento del diagnóstico será preciso revisar el etiquetado de los alimentos manufacturados para asegurarse que no contienen PLV.
¿Dónde y cómo debe realizarse la prueba de adquisición de tolerancia (PAT)?
La PAT la realizaremos entre los 3 y los 12 meses de la exclusión, en hospital o en el domicilio dependiendo de la entidad y de la gravedad de sus manifestaciones clínicas.
Los casos leves y moderados como la proctocolitis, reflujo gastroesofágico (RGE) o cólicos suelen adquirir tolerancia precozmente (entre los 3-6 meses) y se podrá plantear realizarla en domicilio de forma escalonada.
En los casos con síntomas graves o inmediatos, más característicos de la FPIES, será recomendable realizarla en medio hospitalario ante la eventualidad de precisar tratamiento médico y no antes de los 12 meses (incluso puede retrasarse hasta 24 meses entre cada prueba).
Previo a la PAT se planteará realizar prick test o IgE especifica solo en caso de presentar FPIES, sintomatología inmediata o signos de atopia como dermatitis atópica, broncoespasmo de repetición, rinitis alérgica o sensibilización a otros alimentos; dado que estos pacientes tienen más probabilidad de desarrollar una forma IgE mediada tras una exclusión prolongada.
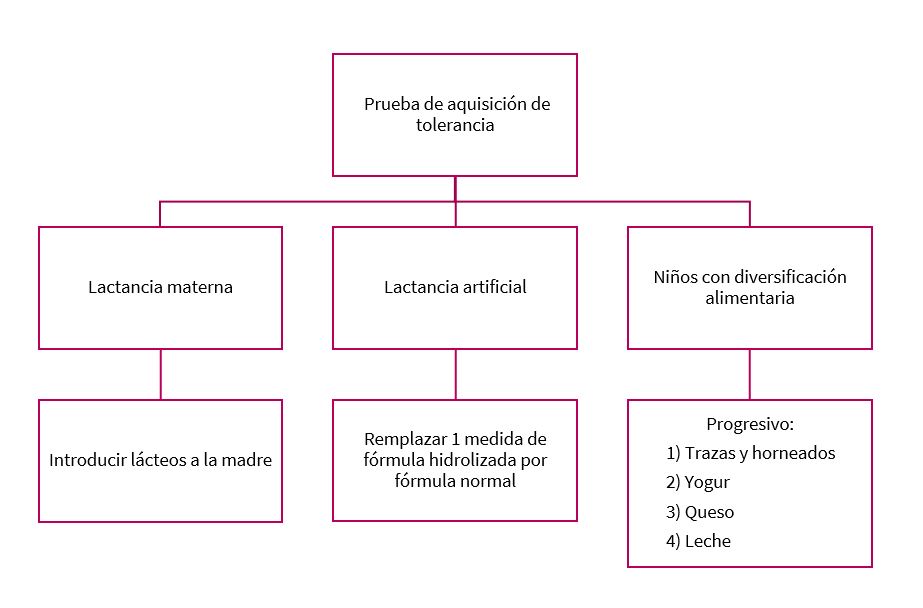
En cuanto a la forma de realizar la PAT, las últimas recomendaciones5 indican (Figura 2):
Figura 2. Prueba de adquisición de tolerancia. Mostrar/ocultar
- En los niños alimentados con LM se recomienda a la madre introducir un lácteo o derivado al día durante la primera semana y, si no reaparecen los síntomas en el bebé, continuar aumentando después progresivamente.
- En los niños alimentados con LA se recomienda cambiar 1 medida de fórmula hidrolizada por fórmula normal al día, al menos en 2 tomas. Si no hay síntomas, se recomienda continuar añadiendo 1 medida al día de forma progresiva.
- En niños más mayores con diversificación alimentaria se puede comenzar escalonadamente de forma semanal y progresiva: 1) se introducirán productos con trazas y horneados (por ejemplo, galletas, bollería, pan con leche); 2) yogur natural; 3) quesos, y 4) leche. Si lo toleran adecuadamente se puede pasar al siguiente escalón. Si en algún momento comenzaran con síntomas se indicará parar en el último escalón que hayan tolerado y mantenerlo.
Durante la realización de la PAT es importante que el niño no introduzca otros alimentos nuevos que puedan confundir la reacción, que no se encuentren con una infección intercurrente que pudiera producir síntomas similares a los observados en la APLV y que se observe hasta 4 semanas la clínica tras la introducción del alimento.
¿Es necesario algún cambio en el calendario vacunal o prescribir adrenalina autoinyectable en pacientes con APLV no IgE mediada?
Dado que, en estos casos, la reacción no está mediada por un mecanismo IgE específico, no se recomienda modificar el calendario vacunal ni la prescripción sistemática de la adrenalina autoinyectable, pues no tiene ningún papel en su tratamiento, ni siquiera en los casos con manifestaciones más graves como la FPIES.
En España, ninguna vacuna contiene PLV, por lo que no sería preciso cambiarlo tampoco en los pacientes con manifestaciones IgE mediadas. La única contraindicación se da en los pacientes que hayan presentado una reacción anafiláctica previa a la administración de la vacuna, que será probablemente causada por los excipientes.
¿Se puede prevenir el desarrollo de la APLV no IgE mediada?
No se ha demostrado que ninguna intervención en la dieta materna, durante el embarazo o en la dieta del lactante, prevenga el desarrollo de la APLV. No existe suficiente evidencia que apoye la retirada de lácteos de la dieta materna, ni la administración de probióticos en el lactante, ni la utilización de FH o FPH en lactantes de riesgo de forma preventiva.
RESOLUCIÓN DEL CASO CLÍNICO
Dado que la clínica consiste en hebras de sangre escasa en un lactante sin repercusión clínica, que ha comenzado recientemente con fórmula adaptada, se establece el diagnóstico de sospecha de APLV no IgE mediada y se decide continuar con LM y cambiar la fórmula adaptada que había iniciado por una extensamente hidrolizada. La sangre en heces disminuye de forma progresiva hasta su desaparición completa al décimo día. A las 3 semanas realizamos la reintroducción de fórmula normal de forma progresiva, y con el cambio del segundo cacito de PLV ya comienza a aparecer de nuevo la hematoquecia, por lo que se da por positiva la prueba de exclusión-provocación y se mantiene la FEH durante 6 meses. En ese momento (10 meses de edad cronológica) realizamos prueba de adquisición de tolerancia de forma progresiva, comenzando con galletas, posteriormente yogures y quesos y finalmente se realiza el cambio de fórmula adaptada cacito a cacito sin clínica alguna, por lo que se considera APLV no IgE mediada en forma de procotolitis alérgica superada, y a partir de entonces continua con dieta libre.
BIBLIOGRAFÍA
- Schoemaker AA, Sprikkelman AB, Grimshaw KE, Roberts G, Grabenhenrich L, Rosenfeld L, et al. Incidence and natural history of challenge-proven cow’s milk allergy in European children - EuroPrevall birth cohort. Allergy. 2015;70:963-72.
- Martorell-Aragonés A, Echeverría-Zudaire L, Alonso-Lebrero E, Boné-Calvo J, Martín-Muñoz MF, Nevot-Falcó S, et al. Position document: IgE-mediated cow’s milk allergy. Allergol Immunopathol (Madr). 2015;43:507-26.
- Grupo Gastrosur-Oeste. Protocolo de hemorragia digestiva baja [Internet]. En: Asociación Madrileña de Pediatría de Atención Primaria [en línea] [consultado el 14/5/2020]. Disponible en: http://www.ampap.es/wp-content/uploads/2014/05/Hemorragia_digestiva_baja_2011.pdf
- Ramos Espada JM. Hemorragia digestiva baja: protocolo diagnóstico-terapéutico. An Pediatría. 2002;57:472-9.
- Espín Jaime B, Díaz Martín JJ, Blesa Baviera LC, Claver Monzón Á, Hernández Hernández A, García Burriel JI, et al. Alergia a las proteínas de leche de vaca no mediada por IgE: documento de consenso de la Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (SEGHNP), la Asociación Española de Pediatría de Atención Primaria (AEPAP), la Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP) y la Sociedad Española de Inmunología Clínica, Alergología y Asma Pediátrica (SEICAP). An Pediatría. 2019;90:193.e1-193.e11.
- Grupo Gastrosur-Oeste. Protocolo de alergia a la proteína de leche de vaca no mediada por IgE. síndrome de enterocolitis inducida por proteínas alimentarias (FPIES). En: Asociación Madrileña de Pediatría de atención Primaria (en línea) [en línea] [consultado el 07/09/2020]. Disponible en: http://www.ampap.es/wp-content/uploads/2019/04/Alergia-a-la-prote%C3%ADna-de-leche-de-vaca-no-mediada-por-IGE.-Sindrome-de-enterocolitis-inducida-Ipor-proteinas-alimentarias-FPIES.pdf
- Koletzko S, Niggemann B, Arato A, Dias JA, Heuschkel R, Husby S, et al. Diagnostic Approach and Management of Cowʼs-Milk Protein Allergy in Infants and Children: ESPGHAN GI Committee Practical Guidelines. J Pediatr Gastroenterol Nutr. 2012;55):221-9.