Hepatitis C en Pediatría
2 Pediatra. CS de Sonseca. Toledo (España).
3 Unidad de Infecciosas. Servicio de Pediatría. Hospital Virgen de la Salud. Toledo (España).
PUNTOS CLAVE
- La hepatitis C es la principal causa de hepatitis crónica en la infancia.
- No existe vacuna eficaz.
- La forma de transmisión más frecuente es la vertical, durante el parto.
- El parto vaginal es seguro y la lactancia materna no debe contraindicarse salvo en situaciones muy concretas.
- El riesgo de infección aguda en el recién nacido hijo de madre RNA virus de la hepatitis C (VHC) positivo se encuentra en torno al 3-5%; y de este porcentaje, hasta un 75-80% pueden adquirir la infección crónica.
- El tratamiento aceptado hasta el momento en niños se basa en el empleo de interferón-peg y ribavirina. Desde principios del 2015 se están empleando nuevos antivirales en la hepatitis C crónica del adulto.
INTRODUCCIÓN
La enfermedad infantil es infrecuente, sin embargo, desde la vacunación universal de la hepatitis B, la hepatitis C es la principal causa de hepatitis crónica en la infancia.
En niños españoles, de 505 casos de hepatitis C registrados hasta 1999, el 51% tenían su origen en una fuente parenteral, el 41% un familiar infectado (la madre) y el 8% carecían de antecedentes.
Desde que se iniciara el cribado transfusional al inicio de los años 90, la forma de transmisión más frecuente es la vertical. En cuanto a la transmisión horizontal, el virus de la hepatitis C es responsable del 90% de las hepatitis transfusionales1.
CASO CLÍNICO
Niña de siete años, nacida en Rumanía y residente en España desde los cuatro años, en seguimiento por astenia y pérdida de peso en los últimos meses. No refiere antecedentes de interés salvo un embarazo no controlado en su país de origen. La exploración física revela la existencia de una leve hepatomegalia. En el estudio básico se solicita una analítica completa con bioquímica, hemograma, estudio de coagulación, perfil férrico y despistaje de celiaquía, observándose una elevación de las transaminasas, con GOT de 356 UI/l y GPT de 585 UI/l, siendo el resto normal. Se solicita una nueva muestra que confirma los resultados anteriores, por lo que se remite a la consulta de Digestivo infantil para un estudio etiológico. En dicha consulta se realiza una ecografía abdominal que muestra hepatomegalia, con un hígado heterogéneo y de bordes mal definidos, así como una nueva analítica, que revela serología positiva para VHC (se detecta RNA de VHC, con anticuerpos anti-VHC positivos), haciéndose el diagnóstico de hepatitis C crónica.
EL PROBLEMA EN NUESTRO MEDIO
La hepatitis C es una de las principales causas de enfermedad hepática y el motivo más frecuente de trasplante hepático en adultos, en EE. UU. y Europa. La causa más frecuente de trasplante hepático en la infancia es la atresia de vía biliar extrahepática, sin embargo, el primer dato no deja de ser relevante ya que los niños con hepatitis C en la infancia serán adultos con hepatitis C crónica en el futuro, y podrán requerir trasplante por ese motivo.
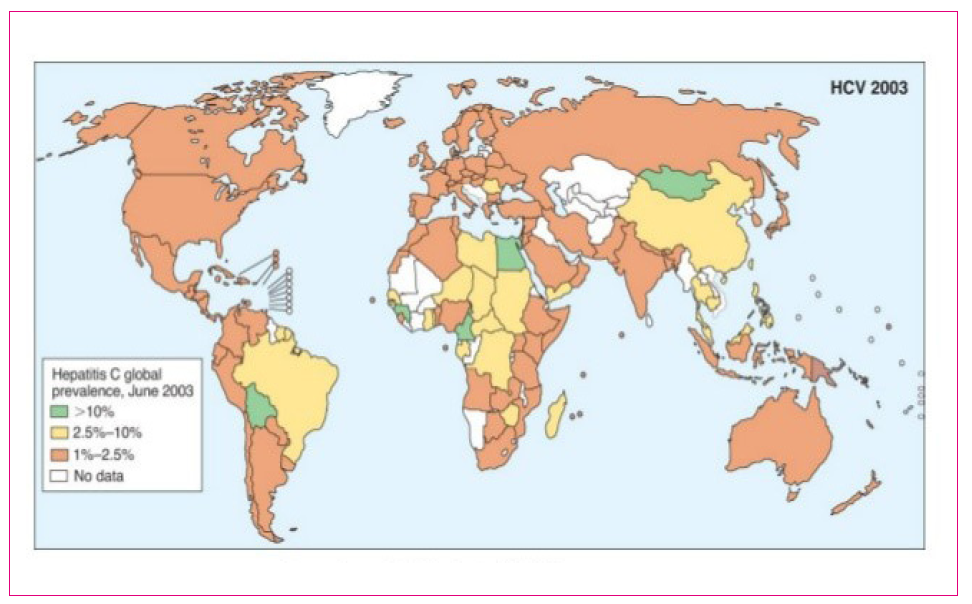
Se estiman 170 millones de personas afectas de hepatitis C en el mundo. España tiene una prevalencia de entre el 1 y el 2,5% (Figura 1). La expansión de la enfermedad tuvo lugar en el siglo XX por el contagio por vía parenteral.
Figura 1. Mapa mundial de prevalencias del virus de la hepatitis C de la Organización Mundial de la Salud (basado en datos de 2003). Mostrar/ocultar
La importancia de la infección crónica por VHC radica en la posibilidad de progresión del daño hepático a lo largo del tiempo a carcinoma hepatocelular y cirrosis.
ORIENTACIÓN CLÍNICA EN LA CONSULTA DE ATENCIÓN PRIMARIA
La hipertransaminasemia en la edad pediátrica tiene un origen muy variado (Tabla 1). Ante este hallazgo es importante confirmar con otra determinación la alteración analítica, y posteriormente realizar el estudio etiológico, que puede iniciarse tanto en la consulta de Atención Primaria como en una consulta especializada2. La causa más frecuente de elevación de enzimas hepáticas es la infección por virus hepatotropos y es lo primero que hay que descartar en esta situación. En este caso es importante preguntar sobre los antecedentes familiares y personales para detectar situaciones de riesgo:
- Hijo de madre con hepatitis C crónica.
- Inmunosupresión.
- Adicción a drogas por vía parenteral.
- Prematuridad
- Necesidad de múltiples cirugías, transfusiones múltiples, hemodiálisis.
Tabla 1. Diagnóstico diferencial de hipertransaminasemia2. Mostrar/ocultar
Tampoco hay que olvidar hacer una exploración física sistemática en busca de datos de hepatopatía crónica: hepatomegalia o hígado pequeño (cirrótico), arañas vasculares, acropaquias, esplenomegalia o circulación colateral.
ESTRUCTURA DEL VIRUS
El virus de la hepatitis C es un virus RNA de cadena lineal, perteneciente a la familia Flaviviridae. Se han descrito seis genotipos distintos, los más frecuentes en Europa son el 1A y el 1B (64%). Los genotipos 2 y 3 tienen mayor tasa de curación espontánea y tras tratamiento.
VÍAS DE TRANSMISIÓN
Existen dos vías de transmisión principales: la vertical y la horizontal3:
Transmisión vertical
La forma más frecuente es la que se produce durante el parto.
El riesgo de transmisión vertical en hijos de madre con hepatitis C crónica (RNA VHC positivo) es del 3-5%, siendo el factor de riesgo más importante la carga viral materna4,5.
El riesgo de cronicidad oscila entre el 75-80% de los casos de infección aguda5.
El modo de parto y si es apta o no la lactancia materna han sido siempre temas muy controvertidos. Según la literatura médica reciente, no existen diferencias estadísticamente significativas en la tasa de transmisión vertical en cuanto a la forma de parto, vaginal o cesárea electiva. Por otro lado, la escasa carga viral en la leche, su inactivación por el pH ácido gástrico y sus beneficios inmunológicos justificarían la recomendación de la lactancia materna en niños nacidos de madres con hepatitis C6.
Transmisión horizontal
El virus de la hepatitis C es responsable del 90% de las hepatitis transfusionales. Los factores de riesgo para hepatitis C horizontal en niños son:
- Transfusión sanguínea antes de 1992.
- Inmunodeprimidos.
- Grandes cirugías.
- Prematuridad y paso por la Unidad de Cuidados Intensivos.
- Hemodiálisis.
- Abuso de drogas por vía parenteral.
- Tatuajes, piercing.
INFECCIÓN AGUDA
Viene definida por la presencia de RNA VHC a los tres meses de edad y en otra determinación separada al menos cuatro meses de la primera y/o persistencia de anticuerpos anti-VHC a partir de los 18 meses de edad (Tabla 2)7.
Tabla 2. Significado serológico. Mostrar/ocultar
Se propone el siguiente cribado de hepatitis C en hijo de madre RNA VHC positivo:
- RNA VHC por PCR a los 3 meses de vida (alto VPN).
- Anticuerpos anti-VHC a los 18-24 meses de vida (alto VPN).
INFECCIÓN CRÓNICA
Viene definida por la presencia de RNA VHC a los tres años desde el momento de la infección (si fue perinatal, desde el nacimiento, es decir, a los tres años de edad del niño)7.
La elevación de transaminasas es más llamativa durante los primeros meses de vida. Solo el 10-20% de los pacientes con hepatitis crónica presentan hepatomegalia.
La carga viral no se relaciona de forma directa con el daño hepático, analítico ni histológico.
TRATAMIENTO
El objetivo del tratamiento es lograr la curación de la enfermedad. La importancia de la infección crónica por el virus de la hepatitis C radica en la posibilidad de progresión del daño hepático a lo largo del tiempo.
La cuestión es decidir el momento más adecuado para el tratamiento. En orden práctico la edad más aconsejable es entre los seis y los diez años.
El tratamiento aceptado hasta el momento en menores de 18 años se basa en el empleo de interferón-peg y ribavirina y la duración del mismo varía en función del genotipo8,9.
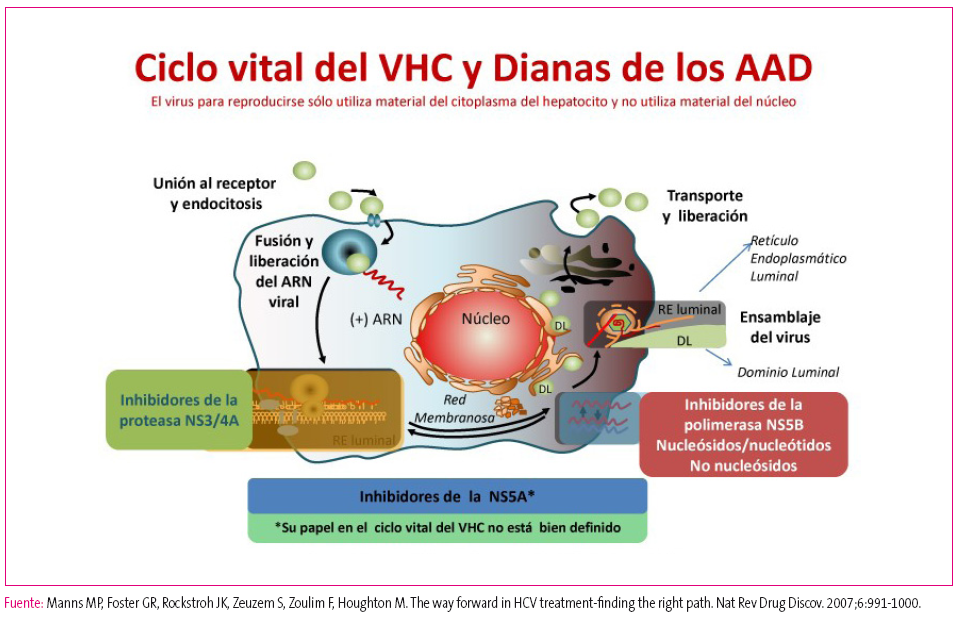
En el primer semestre de 2015 fueron aprobadas tres familias de nuevos antivirales, los llamados antivirales de acción directa (AAD), para el tratamiento de la hepatitis C crónica en mayores de 18 años, lo que ha supuesto un cambio radical en el manejo y pronóstico de esta enfermedad. El tratamiento con los nuevos antivirales es más cómodo (mejora la adherencia del paciente), conlleva menos efectos secundarios y menor tasa de resistencias, y además presenta una alta tasa de curación. Estos fármacos, a diferencia de los fármacos clásicos que basan su actividad en potenciar la respuesta del sistema inmune, inciden en tres fases del proceso replicativo del virus (Figura 2)10,11:
- Inhibidores de la proteasa: terminados en “previr”: simeprevir, paritaprevir.
- Inhibidores de la polimerasa: terminados en “buvir”: sofosbuvir, dasabuvir.
- Inhibidores de la proteína NS5A: terminados en “asvir”: daclatasvir, ombitasvir.
Figura 2. Ciclo vital del VHC y dianas de los antivirales de acción directa (AAD). Mostrar/ocultar
En determinadas situaciones, se recomienda tratar con los fármacos clásicos y no esperar a que los AAD sean aprobados en niños o a que el niño alcance la mayoría de edad. Estas situaciones son12:
- Pacientes con necesidad de trasplante y/o tratamiento inmunosupresor en el futuro.
- Pacientes con enfermedad hepática avanzada.
- Pacientes residentes en zonas donde no está prevista la aprobación de los antivirales nuevos por su escasa accesibilidad.
Los nuevos antivirales emergen como una promesa, y pronto serán una realidad en el tratamiento de la hepatitis C en niños.
BIBLIOGRAFÍA
- Rodrigues Silva L. Hepatitis virales agudas. En: Jara P (ed.). Enfermedad hepática en el niño. Madrid: Tile Von Spain; 2014. p. 205-231.
- Lesmes Moltó M, Albañil Ballesteros MR. Aumento aislado de transaminasas: aproximación diagnóstica. Form Act Pediatr Aten Prim. 2013;6:35-42.
- Goldberg E, Chopra S, O´Donovan DJ. Vertical transmission of hepatitis C virus. En: UpToDate [en línea] [consultado 14/06/2016]. Disponible en: http://www.uptodate.com/contents/vertical-transmission-of-hepatitis-c-virus
- Pawlovska M, Domagalski K, Pniewska A, Smok B, Halota W, Tretyn A. What´s new in hepatitis C virus infections in children? World J Gastroenterol. 2015;21:10783-9.
- Maureen M Jonas. Hepatitis C virus infection in children. En: UpToDate [en línea] [consultado 14/06/2016]. Disponible en: http://www.uptodate.com/contents/hepatitis-c-virus-infection-in-children
- Madruga Sevilla P, Aguar Carrascosa M, Pereda Pérez A, Modesto Alapont V, Montañés Sánchez A, Torres Martínez E, et al. Estudio retrospectivo de factores de riesgo de transmisión vertical de infección por virus hepatitis C. An Pediatr (Barc). 2012;76:336-42.
- Jara P. Hepatitis crónica C. En: Jara P (ed.). Enfermedad hepática en el niño. Madrid: Tile Von Spain; 2014. p. 253-74.
- Wirth S, Kelly D, Sokal E, Socha P, Mieli-Vergani G, Dhawan A, et al. Guidance for clinical trials for children and adolescents with chronic hepatitis C. J Pediatr Gastroenterol Nutr. 2011;52:233-7.
- Hierro L, Fischler B. Treatment of pediatric chronic viral hepatitis B and C. Clin Res Hepatol Gastroenterol. 2014;38:415-8.
- Ministerio de Sanidad, Servicios Sociales e Igualdad. Estrategia terapéutica para la hepatitis crónica por el virus de la hepatitis C en el Sistema Nacional de Salud. Pleno del Consejo Interterritorial del SNS el 26 de marzo de 2015. Disponible en: http://www.msssi.gob.es/ciudadanos/enfLesiones/enfTransmisibles/docs/plan_estrategico_hepatitis_C.pdf
- Documento del II Consenso español sobre el tratamiento de la hepatitis C. En: Asociación Española para el Estudio del Hígado [en línea] [consultado el 14/06/2016]. Disponible en: http://aeeh.es/wp-content/uploads/2015/04/II-Conferencia-de-consenso-sobre-el-tratamiento-de-la-hepatitis-C-de-la-AEEH.pdf
- Granot E, Sokal E. Hepatitis C virus in children: deferring treatment in expectation of direct-acting antiviral agents. IMAJ. 2015;17:707-11.