La litiasis renal y la prelitiasis en la edad pediátrica
2 Pediatra. CS de Laviana. Pola de Laviana. Asturias (España).
3 Hospital Nuestra Señora de La Candelaria. Universidad de La Laguna. S.C.Tenerife (España).
PUNTOS CLAVE
- La nefrolitiasis es una enfermedad que comienza en la infancia.
- La prevalencia de la urolitiasis ha ido en aumento en las últimas décadas.
- El diagnóstico precoz es necesario para prevenir complicaciones a largo plazo.
- La mayoría de los cálculos en los niños se componen de oxalato y de fosfato cálcico, y se asocian a menudo con una o varias alteraciones metabólicas.
- En todos los niños con litiasis o prelitiasis está indicada una evaluación metabólica urinaria.
- La alteración metabólica más frecuente es la hipercalciuria idiopática.
- El cociente calcio:creatinina es de gran importancia en el despistaje de los niños con orina con potencial litogénico.
- El estudio de los progenitores es muy importante, dadas las bases genéticas de las anomalías metabólicas causantes de cálculos.
- La prevención, dado el elevado porcentaje de recidivas, debe ser un objetivo irrenunciable para el pediatra.
- La litotricia extracorpórea es un método con excelentes resultados, incluso en la edad pediátrica.
- Es preciso esterilizar la orina antes de practicar una litotricia extracorpórea, una nefrolitotomía percutánea o una ureteroscopia flexible.
INTRODUCCIÓN Y DEFINICIONES
Llamamos litiasis a la formación de cálculos en una cavidad o conducto del organismo, especialmente en las vías biliares y/o en las urinarias.
La nefrolitiasis consiste en la presencia de cálculos en las vías urinarias como consecuencia de un proceso complejo en el que intervienen desajustes fisiológicos de tipo bioquímico, caracterizados por el aumento de factores promotores y la disminución de factores inhibidores de la cristalización.
La prelitiasis es una situación clinica en la que algunos niños portadores de alteraciones metabólicas de base genética producen una orina de características tales que condicionan un mayor riesgo de formar cálculos en la propia infancia o en la edad adulta.
El propósito de esta revisión es realizar una actualización de una circunstancia patológica poco prevalente, pero que se ha incrementado en las últimas décadas y que puede tener repercusiones, especialmente en la calidad de vida de los sujetos afectos. En ocasiones, además, puede repercutir sobre la función renal a largo plazo. De ahí la importancia de un diagnóstico precoz, tanto en la infancia, donde suele comenzar la enfermedad, como en la edad adulta.
EPIDEMIOLOGÍA
La epidemiología es uno de los aspectos más interesantes de la enfermedad litiásica. En España, la dificultad para realizar estudios epidemiológicos sobre urolitiasis radica en la falta de registros sanitarios oficiales, por lo que siguen siendo los registros hospitalarios la fuente más empleada para la obtención de datos sobre la frecuencia y prevalencia de la enfermedad. Para abordar este problema se ha creado, junto con la Asociación Española de Nefrología Pediátrica y la Universidad de las Islas Baleares, a través del Laboratorio de Investigación en Litiasis Renal, un registro de litiasis renal pediátrica para todo el territorio español. Algunos estudios españoles consultados sobre el tema se resumen en la Tabla 1.
Tabla 1. Datos epidemiológicos en estudios españoles. Mostrar/ocultar
La nefrolitiasis endémica infantil, con características similares a las descritas en Europa en el siglo XIX, se extiende por áreas de Turquia, Irán, India, China, Indochina e Indonesia3. Estudios epidemiológicos recientes han demostrado que la incidencia de la litiasis pediátrica está aumentando en Occidente3. Aproximadamente un 7% de todos los cálculos urinarios en EE. UU. se producen en niños menores de 16 años4. Los datos epidemiológicos correspondientes a dos series procedentes de EE. UU. aparecen en la Tabla 2.
Tabla 2. Datos epidemiológicos en dos series de EE. UU. Mostrar/ocultar
LA FORMACIÓN DE LOS CÁLCULOS. ANOMALÍAS METABÓLICAS CAUSANTES DE CÁLCULOS
La etiología de la urolitiasis es multifactorial e implica factores genéticos, ambientales, raciales y estructurales, además de mecanismos físicoquímicos complejos7. La formación y el crecimiento de los cálculos requiere de la sobresaturación de ciertos iones en la orina. Los factores más importantes que determinan la solubilidad en la orina y la probabilidad de sobresaturación de esos iones con la correspondiente cristalización son:
- El volumen total de orina.
- La concentración de las sustancias favorecedoras de la cristalización.
- La concentración de las sustancias inhibidoras de la cristalización.
- El pH urinario.
En nuestro país, las anomalías metabólicas representan desde un 25 hasta un 65%, según las series1,2. El pH de la orina es importante en la formación de algunos tipos de cristales, tales como la cistina y el ácido úrico, porque son más propensos a agregarse en la orina ácida, mientras que el fosfato de calcio es más probable que precipite en la orina alcalina. La solubilidad del oxalato de calcio no se afecta, apreciablemente, por los cambios en el pH urinario si están dentro del pérfil fisiologico8,9. Todos los tipos de cálculos son menos propensos a formarse cuando la orina es diluida.
El proceso de la cristalización
La cristalización comienza con la formación de un núcleo, que puede estar formado a partir de restos celulares, cilindros hialinos o de otros cristales, dentro del proceso que se conoce con el nombre de nucleación heterogénea. Estos núcleos se localizan en las placas de Randall, que son excrecencias o proliferaciones sobre placas de apatita en las papilas renales, y surgen en la membrana basal de la porción fina del asa de Henle, pasando a través del intersticio, hacia la membrana basal del endotelio papilar10. Al quedar expuestas, cuando las células endoteliales son lesionadas, se convierten en las bases para la cristalización del oxalato de calcio.
Estos nidos son críticos en la formación de la mayoría de los casos idiopáticos de cálculos de oxalato cálcico que están formados como monohidrato (whewellita) o como dihidrato (whedellita) que, a menudo, se mezclan con pequeñas cantidades de fosfato de calcio11,12.
Los cálculos de oxalato cálcico y de fosfato cálcico representan alrededor del 75% de todos los que se eliminan en los niños2,13. En el Reino Unido y otros países europeos, el 75% de los cálculos en los niños están compuestos de matriz orgánica y estruvita (fosfato amónico magnésico) (Figura 1) y están asociados con la infección por Proteus y anomalías del tracto urinario. Curiosamente, no ocurre así en EE. UU. ni en los países escandinavos, donde los cálculos asociados a infecciones son raros. En EE. UU., un 75% de los mismos están constituidos por oxalato de calcio y fosfato. Solo entre el 15 y el 25% son favorecidos por infecciones13-14.
Figura 1. Detalle de un cristal de estruvita (fosfato amónico magnésico en cuyas caras se observan las marcas en “Y” que permiten su rápida identificación, junto con pequeñas zonas de esferulitos de hidroxiapatita Mostrar/ocultar
Anomalías metabólicas favorecedoras de la formación de cálculos cuando su concentración es elevada
Las cuatro causas más importantes de formación de cálculos, cuando su concentración está elevada, son el calcio, el oxalato, la cistina y el ácido úrico1,2,15.
Hipercalciuria
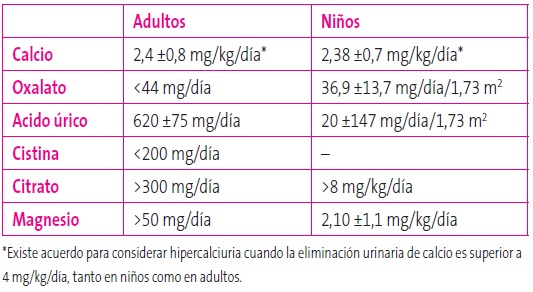
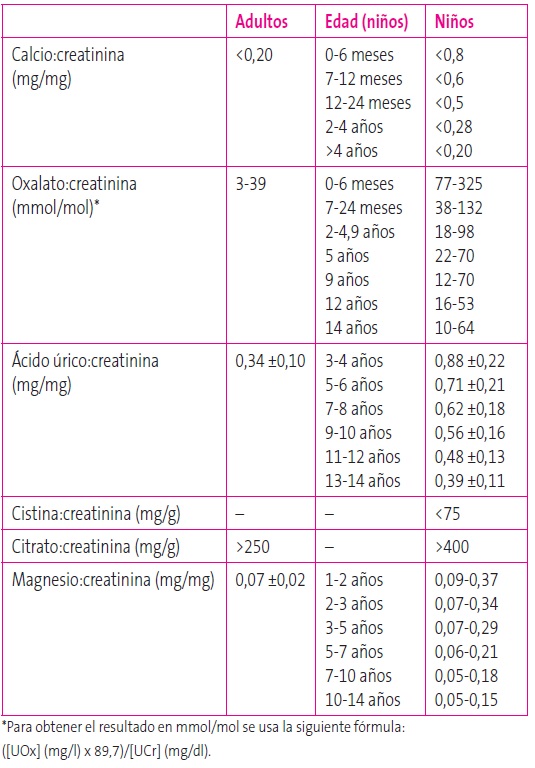
La hipercalciuria se define como una excreción de calcio en orina de 24 horas superior a 4 mg/kg/día, tanto en niños como en adultos. En los niños menores de tres meses, el límite superior de la normalidad está en los 5 mg/kg/día14. En la actualidad, cada vez se usan más los cocientes urinarios por su facilidad en la recogida de las muestras, especialmente en la infancia, y porque las concentraciones, especialmente las de calcio y citrato, pueden variar en distintos momentos del día (Tabla 4).
La causa más habitual de litiasis en niños y adultos es la hipercalciuria idiopática, definida como aquella que ocurre en ausencia de hipercalcemia y de otras causas identificables de hipercalciuria secundaria1,2,13.
La hipercalciuria idiopática es de origen genético. No se considera una enfermedad en sí misma, sino una anomalía metabólica, puesto que, en muchas ocasiones, no se asocia con clínica ni con la propia formación de cálculos. No se han identificado genes causales, aunque parece que la transmisión es de carácter autosómico dominante con penetrancia incompleta1,14.
El mecanismo fisiopatológico es muy complejo. Se han descrito dos posibles mecanismos. En el primero, lo primario sería la existencia de un incremento en la producción de IL-1 y otras citocinas por parte de los monocitos que estimularían la resorción ósea y secundariamente la producción de prostaglandina E2 (PGE2) que, a su vez, incrementaría la de calcitriol. La hipercalciuria se ocasionaría, por tanto, por un incremento de resorción ósea y por un aumento de la reabsorción intestinal de calcio debido al efecto del calcitriol. Junto a ello, una dieta rica en sal o en proteínas de origen animal acrecentaría, aún más, la calciuria. El segundo mecanismo se basa en los hallazgos realizados en ratas hipercalciúricas, en las que se ha demostrado que existe un incremento en el número de receptores de la vitamina D (VDR) tanto en el intestino como en el hueso, lo que induciría un incremento de la capacidad funcional de los complejos calcitriol-VDR. Se ha comprobado que en estos animales existe una hiperrespuesta de los VDR a mínimas dosis de calcitriol, lo que implica que no son necesarios niveles muy elevados del mismo para amplificar su respuesta e incrementar sobremanera la calciuria.
La hipercalciuria secundaria a hipercalcemia puede obedecer a un aumento de la resorción ósea (hiperparatiroidismo, hipertiroidismo, inmovilización prolongada, acidosis metabólica, enfermedad metastásica) o a hiperabsorción digestiva (hipervitaminosis D)14. Las hipercalciurias secundarias sin hipercalcemia se observan, preferentemente, en algunas tubulopatías (acidosis tubular tenal distal, síndrome de Bartter, hipomagnesemia con hipercalciuria y nefrocalcinosis) (Figuras 2 y 3).
Figura 2. Algoritmo diagnóstico inicial de la hipercalciuria. Mostrar/ocultar
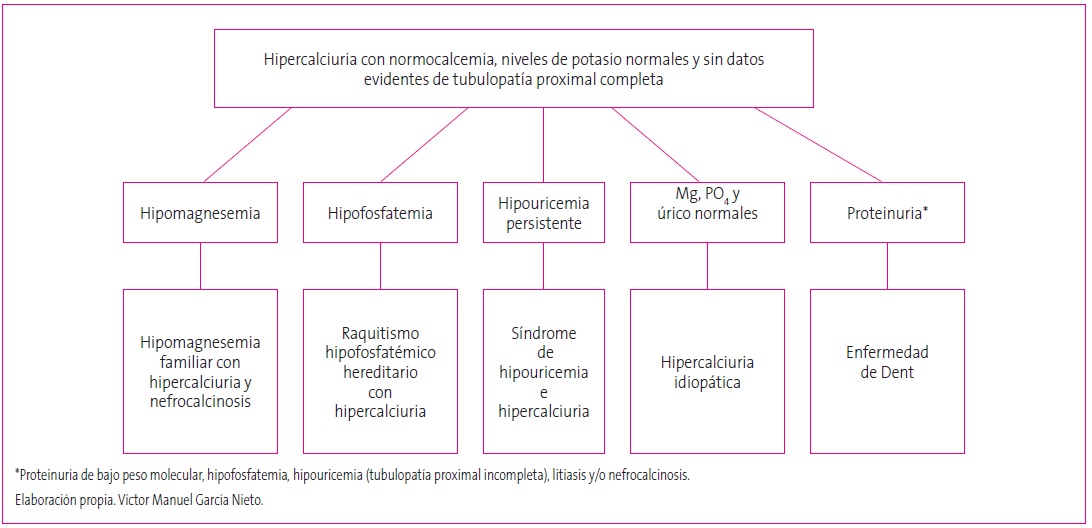
Figura 3. Algoritmo diagnóstico de la hipercalciuria con normocalcemia, niveles de potasio normales y sin datos evidentes de tubulopatía proximal completa. Mostrar/ocultar
Hiperoxaluria
El ácido oxálico es un metabolito de origen hepático que se excreta por los riñones. Tan solo entre el 10 y el 15% del oxalato procede de la dieta. La hiperoxaluria puede ser resultado de un aporte alimentario elevado, de hiperabsorción intestinal (como en el síndrome del intestino corto, diarreas crónicas) o de un defecto congénito del metabolismo hepático del oxalato13,14.
En la hiperoxaluria primaria existe un déficit funcional de la actividad de una de tres de las enzimas hepáticas que intervienen en el metabolismo del oxalato. Se comprueba depósito de oxalato en diversos órganos y, especialmente, en el riñón. Los pacientes suelen padecer una enfermedad renal crónica que, en muchos casos, es terminal. En este caso, el tratamiento es el trasplante combinado de hígado y de riñón.
Hiperuricosuria
El ácido úrico es el producto final del metabolismo de las purinas. Promueve la cristalización de oxalato de calcio al favorecer el proceso de epitaxia, que consiste en que una base de cristal de un determinado material permite el crecimiento de un segundo mineral que se encuentra en la misma orientación cristalina.
Los cálculos de ácido úrico representan el 4-8% de los cálculos urinarios en los niños, y la hiperuricosuria es su principal causa.
La formación de cálculos de ácido úrico depende, principalmente, de un pH ácido urinario. La disociación y solubilidad del ácido úrico se reducen mucho cuando el pH es inferior a 5,8. A medida que el pH se torna más alcalino, los cristales de ácido úrico se hacen más solubles y se reduce el riesgo de formación de cálculos.
En la forma familiar o idiopática de hiperuricosuria, los niños suelen presentar unas concentraciones séricas normales de ácido úrico. En otros casos, puede estar causada por una producción excesiva de ácido úrico secundaria a defectos congénitos del metabolismo, trastornos mieloproliferativos u otras causas de destrucción celular. La hiperuricosuria también puede estar causada por un aporte elevado de purinas y de proteínas. Un elevado porcentaje de los niños que tienen hiperuricosuria idiopática (entre el 20 y el 40%), presenta, concomitantemente, hipercalciuria asociada.
Cistinuria
La cistinuria es la causa de entre el 2 y el 6% de todos los cálculos urinarios en los niños. La cistinuria es un trastorno autosómico recesivo de penetrancia incompleta, que se caracteriza por la incapacidad de los túbulos proximales renales para reabsorber cuatro aminoácidos básicos, a saber, cistina, ornitina, lisina y arginina. De estos cuatro aminoácidos, tan solo la cistina tiene una solubilidad escasa en la orina, por lo que únicamente pueden formarse cálculos de cistina en el caso de una excreción excesiva urinaria. La solubilidad de la cistina depende del pH, de modo que su precipitación se produce a partir de unos valores de pH menores de 7. Otras alteraciones metabólicas, tales como la hipercalciuria, la hipocitraturia y la hiperuricosuria, pueden acompañar a la cistinuria, por lo que pueden dar lugar a la formación de cálculos de composición mixta16.
Anomalías metabólicas favorecedoras de la formación de cálculos cuando su concentración es reducida
El citrato, el magnesio, el pirofosfato, ciertos glucosaminoglucanos, la nefrocalcina y el fitato actúan inhibiendo la formación de cristales de oxalato de calcio y del fosfato de calcio. Por tanto, cuando sus niveles son bajos, se favorece la formación de cristales.
Hipocitraturia
El citrato actúa como un inhibidor de la formación de cálculos en la que interviene el calcio formando un complejo soluble, lo que disminuye la disponibilidad del calcio iónico libre necesario para la cristalización de oxalato o de fosfato cálcicos. El citrato, también, actúa como un inhibidor directo de la agregación de cristales de calcio y de su crecimiento.
Por tanto, un citrato urinario reducido puede ser una causa importante de litiasis cálcica. La hipocitraturia suele aparecer en ausencia de síntomas coexistentes o trastornos metabólicos conocidos. También puede surgir en el seno de casos de acidosis metabólica, acidosis tubular distal, síndromes diarreicos y en la fibrosis quística.
Las cifras normales de la citraturia en niños tienen una gran dispersión por edad y sexo. La citraturia puede expresarse en mg/kg/24 horas, ya que estos valores no se modifican con la edad17,18. No obstante, lo más práctico es expresar la eliminación urinaria de citrato como cociente con respecto a la creatinina, ya que, como hemos indicado más arriba, la citraturia varía en distintos momentos del día (es más reducida por la noche, es decir, la que corresponde a la primera orina del día) (Tabla 4).
Hipomagnesuria
El magnesio forma complejos con el oxalato, con lo que se reduce la supersaturación del oxalato cálcico. Además, los complejos de oxalato magnésico reducen la absorción intestinal de oxalato. A concentraciones fisiológicas de oxalato, el magnesio reduce tanto las tasas de nucleación como las de crecimiento de los cálculos. Se ha descrito hipomagnesuria en pacientes con diarrea crónica, malabsorción intestinal, enfermedad inflamatoria intestinal y resección intestinal.
Litiasis de origen infeccioso (cálculos de estruvita)
En algunas series, los cálculos relacionados con infecciones constituyen entre el 15 y el 25% de los cálculos urinarios en los niños13. En las series españolas representan entre un 7 y un 33% de los casos2. Las bacterias capaces de producir la enzima ureasa (Proteus, Klebsiella, Pseudomonas) son responsables de la formación de estos cálculos. El Proteus puede estar implicado hasta en el 55% de esos casos1.
La ureasa convierte la urea en amoniaco y bicarbonato, de modo que alcaliniza la orina y, además, transforma el bicarbonato en carbonato. Entonces, en ese medio alcalino se forman fosfatos triples que dan lugar a un entorno supersaturado de fosfato amónico magnésico (Figura 1) y carbonato-apatita16.
Malformaciones de las vías urinarias
Las anomalías genitourinarias, como la estenosis pieloureteral, los dobles sistemas, las válvulas uretrales de uretra posterior, etc., se encuentran aproximadamente en el 30% de los niños con urolitiasis. Solo del 1 al 5% de los niños con anomalías urológicas desarrollan cálculos. Tradicionalmente, se ha indicado que la obstrucción funcional o anatómica predispone a los niños a la formación de cálculos por la estasis de la orina y la infección. No obstante, muchos niños que han nacido con malformaciones urinarias son portadores de anomalías metabólicas causantes de cálculos, especialmente hipercalciuria e hipocitraturia14. En los últimos años, se ha descrito que esas anomalías son de origen genético, es decir, uno de los progenitores del paciente es portador de la misma anomalía metabólica y existe, al mismo tiempo, una alta frecuencia de urolitiasis en los miembros de la familia pertenecientes a la primera y/o la segunda generaciones.
Urolitiasis endémica
En la litiasis endémica, los cálculos son de localización vesical, al contrario que en los de los países occidentales, en los que predomina la ubicación renal. Los cálculos están constituidos por urato de amonio y ácido úrico. Se han relacionado con la malnutrición en edades tempranas de la vida y con el destete temprano y la adopción de una dieta de cereales y arroz, pobre en proteínas y fosfato3,13. En un estudio tunecino, en el 40% de los casos se involucraron simultáneamente factores nutricionales, metabólicos e infecciosos. Los cálculos contenían un núcleo compuesto de urato de amonio sin estruvita16.
Otras causas
Como se ha indicado antes, la fibrosis quística puede ser causa de cálculos en las vías urinarias o en los riñones. La causa es la hipocitraturia, aunque, en algunos casos, se han observado hiperuricosuria e hiperoxaluria19. La dieta cetógena es una causa rara de litiasis en niños con epilepsias intratables; la prevalencia en estos casos es de un 3-10%20. Los quistes renales simples, entidades poco frecuentes en la práctica pediátrica, también pueden asociarse a litiasis renal, ya que un 63,6% de estos niños tienen hipercalciuria e hipocitraturia, asimismo, de origen genético21. El cambio climático es un factor que puede tener importancia en el futuro. El número de estadounidenses que vivirán en zonas geográficas de riesgo elevado de calculosis pasará de un 40% en el año 2000 a un 56% en el 2050, y llegará a un 70% en el año 20953,22. La inmovilización prolongada es otra de las causas a reseñar y puede estar presente hasta en un 10% de los casos1,2; su causa es la hipercalciuria causada por un incremento de la resorción ósea. Las transgresiones dietéticas que, con mucha frecuencia, ocurren en los países desarrollados, pueden producir cambios bioquímicos urinarios que originan un ambiente fisicoquímico que favorece la cristalización; en general, se acepta como dieta litógena aquella que ofrece una contribución reducida de líquidos y/o un aporte excesivo de alimentos ricos en calcio, proteínas animales, oxalato y sal. Algunos trastornos digestivos, como las diarreas crónicas, la celiaquía, la enfermedad de Crohn o la colitis ulcerosa, pueden favorecer la formación de cálculos renales; en estos procesos, se produce una importante pérdida intestinal de agua, electrolitos, álcalis y calcio, con la aparición de una orina concentrada y ácida, asociada a una hipocitraturia y a una hiperoxaluria entérica. Por último, debe tenerse en cuenta que, en algunos pacientes, el primer episodio de litiasis renal puede ser la expresión de una enfermedad sistémica, como el hiperparatiroidismo primario, la sarcoidosis o tumores de alto recambio celular como los linfomas (síndrome de lisis tumoral)15.
MANIFESTACIONES CLÍNICAS
Aunque más del 90% de los niños menores de 14 años tienen síntomas, los típicos del adulto son poco frecuentes en la infancia. Cuanto más pequeño es el niño, tanto menos específica es la sintomatología14.
El síntoma más importante es el dolor producido por la circulación del cálculo por las vías urinarias. En el lactante se puede manifestar como llanto inconsolable, por lo que es difícil de diferenciar del cólico15. El dolor en el flanco o abdominal, y también el dolor abdominal recurrente, así como la hematuria, están presentes en un 56% de los niños menores de cinco años de edad2,23-25. El dolor típico del adulto solo se encuentra en los adolescentes15. También pueden tener fiebre si existe una infección urinaria asociada.
Considerando todas las edades, la hematuria macro- o microscópica está presente en un 90% de los niños con litiasis y puede acompañarse o no de dolor14,15.
Por otra parte, se sabe que la hipercalciuria idiopática, la causa más frecuente de cálculos renales a cualquier edad, puede debutar en la infancia con síntomas que pueden no estar estrictamente relacionados con el paso de los cálculos por las vías urinarias2,26,27 (véase la sección “Prelitiasis” en este artículo).
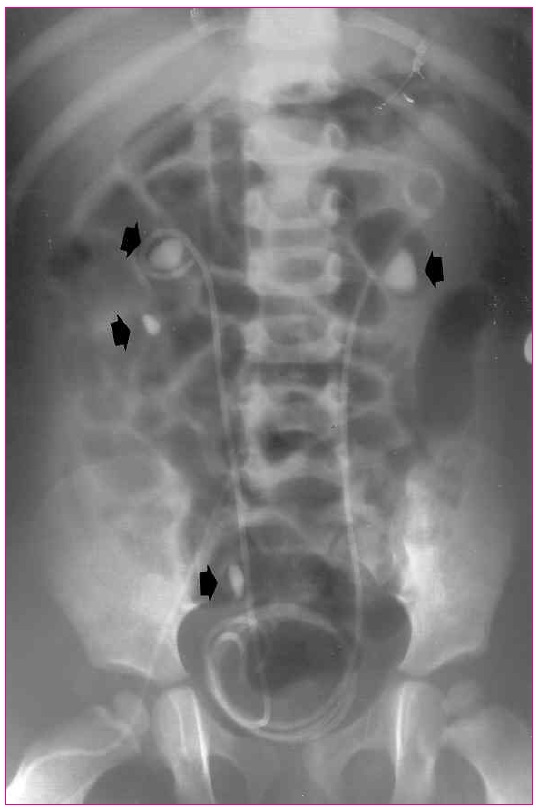
El inicio como una infección de las vías urinarias y los hallazgos radiológicos casuales pueden llegar a representar hasta un 45% de los casos en niños menores de cinco años, y solo en un 15% en los niños de 12 a 16 años de edad. Muy raramente, un paciente litiásico puede debutar en forma de una obstruccion urinaria aguda14 (Figura 4).
Figura 4. Paciente diagnosticada de oxalosis que, con cuatro años, padeció una insuficencia renal aguda obstructiva coincidiendo con un proceso febril agudo debido a un enclavamiento de sendos cálculos en ambas uniones pieloureterales (flechas negras superiores). En el lado derecho se observa, además, un cálculo en el caliz inferior y otro en el trayecto ureteral. Se observan, asimismo, dos cateteres pigtail que se colocaron para resolver el proceso obstructivo agudo Mostrar/ocultar
DIAGNÓSTICO
La evaluación del niño debe ir dirigida a identificar los factores fisicoquímicos, anatómicos y genéticos que predisponen a la formación de cálculos13. Cada uno de los datos obtenidos del paciente a partir de las historia clínica, los estudios de imagen, el análisis del cálculo, el estudio metabólico y el estudio fisicoquímico de la orina, muestra una faceta diferente de un mismo proceso, por lo que todos deben ser valorados individualmente15.
Anamnesis
Se deben investigar los factores familiares, por el peso que tienen las alteraciones metabólicas de origen genéticoen la litiasis infantil.
Es necesario realizar una historia dietética detallada con especial énfasis en la ingesta de líquidos, sal, vitaminas (C, D), suplementos minerales y dietas especiales.
Debe descartarse la ingesta de medicamentos, especialmente corticoides, diuréticos, inhibidores de la proteasa (indinavir) y anticonvulsivantes (topiramato, zonisamida).
Deben conocerse los antecedentes de prematuridad, anomalías o malformaciones del tracto urinario, infecciones urinarias, malabsorción intestinal e inmovilización prolongada14.
Examen físico
Deberá ser minucioso. Es muy útil para conocer las características del dolor abdominal (difuso, localizado, puño percusión renal, etc.). Siempre se debe valorar, además, si existen signos o síntomas asociados indicativos de una enfermedad constitucional, como los síndromes malformativos. Se medirán el peso, la talla y la presión arterial15.
Pruebas complementarias
La sospecha de la litiasis puede partir de una simple tira reactiva en la orina que muestre una hematuria microscópica o un pH alcalino.
La realización de una ecografía debe ser el siguiente paso, ya que tiene una sensibilidad de un 84%23,24 (Figuras 5 y 6). En los cálculos situados en el riñón puede llegar al 90%, pero la sensibilidad es muy pobre si los cálculos se situan en las vías urinarias y su tamaño es menor de 5 mm14.
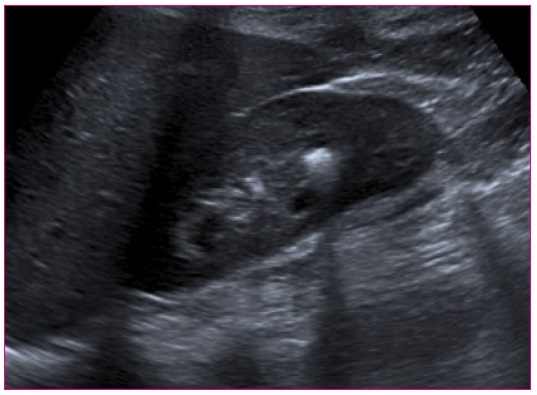
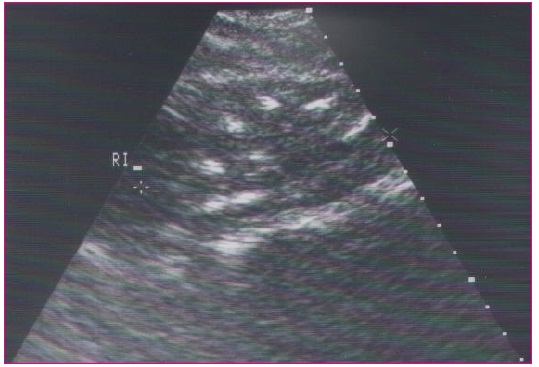
Figura 5. Paciente de nueve años de edad con hipercalciuria e hipocitraturia. Se observa un cálculo de 0,9 cm con la sombra sónica Mostrar/ocultar
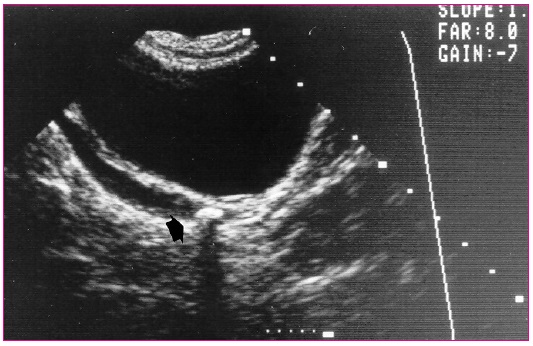
Figura 6. Cálculo ubicado en la unión vesicoureteral. Mostrar/ocultar
La radiografía simple de abdomen puede ayudar, porque un 90% de los cálculos tienen algún grado de calcificación (Figura 4), pero los de pocos milímetros de diamétro son difíciles de visualizar, sobre todo en el uréter. Por todo esto, la sensibilidad de la radiografía no supera el 54%24,28.
En el caso de que no se identifiquen cálculos, pero persistan los síntomas, puede estar indicada la realización de una tomografía computarizada (TC) helicoidal. Es segura y rápida y tiene una sensibilidad del 97% y una especificidad del 96%16.
Otras pruebas diagnósticas complementarias (urografía endovenosa, gammagrafía y resonancia magnética) se indicarán de forma individualizada en función de los hallazgos ecográficos y de las malformaciones asociadas. La urografia está poco indicada en niños. Se restringiría para diagnosticar el riñón en esponja (enfermedad de Cacci-Ricci) y en aquellos casos en los que se deba estudiar la anatomía calicial para practicar cirugía percutánea o abierta4,18. En pacientes con obstrucción renal y riñón excluido, la urorresonancia con gadolinio puede mostrar imágenes muy demostrativas28.
Estudio de la función renal e identificación de las anomalías metabólicas causantes de cálculos
-
Función glomerular: para valorarla se deben determinar las concentraciones de urea y creatinina en sangre, y calcular el filtrado glomerular renal (FGR) con las fórmulas aceptadas para su uso en la edad pediátrica29. No es necesaria una recogida de orina de 24 horas. De acuerdo con la mayoría de las sociedades científicas, aconsejamos utilizar la ecuación de Schwartz-IDMS para la estimación del FG: Schwartz-IDMS, 2009, (ml/min/1,73 m2): 0,413 × (talla/Cr).
Esta ecuación solo es válida para valores de creatinina obtenidos mediante métodos con trazabilidad a IDMS.
Los valores del filtrado glomerular estimado se informarán con el valor obtenido si son inferiores a 75 ml/min/1,73 m2 y en caso contrario como >75 ml/min/1,73 m2.
Hay que tener en cuenta que las ecuaciones basadas en creatinina no deben utilizarse cuando la función renal no es estable, ni tampoco en niños con desviaciones importantes del índice de masa corporal, enfermedades musculares o desnutrición.
En el caso de obtenerse un FGR límite, debería determinarse la cistatina C. Además, es muy conveniente calcular el cociente microalbúmina:creatinina en la primera orina del día (la cifra normal por encima de cuatro años es <3 µg/µmol [30 mg/g]).
- Las anomalías metabólicas causantes de cálculos pueden medirse en orina de 24 horas o en muestras de orina aislada. En la Tabla 3 se muestran los valores de normalidad en orina de 24 horas, y en la Tabla 4, los valores de los cocientes calculados con respecto a la creatinina en orina aislada, de las seis causas metabólicas causantes de cálculos que se determinan habitualmente en los laboratorios de nuestro medio (niños y adultos). En el caso particular del ácido úrico, suele calcularse el índice de excreción, por lo que debe determinarse tanto en sangre como en orina. La fórmula es: ([ácido úrico]u x [creatinina]p)/[creatinina]u. Se consideran elevados unos valores superiores a 0,53 mg/100 ml FGR14.
Tabla 3. Valores de referencia de la eliminación urinaria en orina de 24 horas de las principales anomalías metabólicas causantes de cálculos. Mostrar/ocultar
Tabla 4. Valores de referencia de la eliminación urinaria en orina aislada de las principales anomalías metabólicas causantes de cálculos. Mostrar/ocultar
En el momento actual, en niños, algunos de nosotros preferimos determinar los cocientes urinarios en dos muestras de orina recogidas en dos momentos del día: de noche y en la primera orina de la mañana. La razón de esto último es que la concentración de, al menos, calcio y citrato varian a lo largo del día. En este sentido, la primera orina del día es la más sensible30.
PRELITIASIS
Desde principios de los 80, los pediatras hemos aprendido a identificar a los niños portadores de anomalías metabólicas causantes de cálculos, en un momento en el que aún no les ha dado tiempo a fomarlos. Esto es particularmente cierto con las dos causas más frecuentes de los mismos, la hipercalciuria idiopática y la hipocitraturia. La hipercalciuria es de origen genético, por tanto, uno de los dos progenitores es portador de la misma anomalía, haya tenido o no síntomas de enfermedad litiásica. Los niños con hipercalciuria pueden debutar con síntomas o signos como hematuria macro- o microscópica, disuria estéril, polaquiuria, urgencia miccional, incontinencia urinaria, enuresis nocturna, orinas turbias, dolor abdominal recurrente “no típico de cólico renal” o leucocituria estéril2,26,27. La hipocitraturia es una cuestión pendiente pues, si bien en ocasiones se reconoce su causa, en otras se desconoce y puede coincidir o no con la hipercalciuria. Así, con mucha frecuencia, se observa que los niños con hipercalciuria idiopática, al acercarse a la adolescencia, normalizan la eliminación urinaria de calcio y muestran, entonces, hipocitraturia. Otras veces, los padres de niños con hipercalciuria que han eliminado cálculos son portadores de hipocitraturia. Parece, por tanto, como si ambas anomalías metabólicas tuvieran un origen común.
El diagnóstico de la condición de prelitiasis es, pues, una versión sofisticada de la medicina preventiva, puesto que tras su detección se pueden tomar medidas dietéticas y/o farmacológicas para evitar el desarrollo de la enfermedad litiásica.
La forma más sencilla de despistaje de la prelitiasis es la determinación del cociente calcio:citrato en primera orina del día. La orina es particularmente litógena cuando existe un desequilibrio entre el componente favorecedor (calcio) y el protector (citrato). Este desequilibrio es más patente de noche, puesto que, junto al aumento de la osmolalidad urinaria por la falta de líquidos, durante la misma, se elevan fisiológicamente los niveles de hormona antidiurética (ADH), y se suma, en muchos casos, un incremento de la calciuria por un cierto incremento de la resorción ósea y una reducción de la citraturia como consecuencia de la acidosis fisiológica leve, que es consecuencia de la formación de cetoácidos por la falta de ingesta. Por ello, la primera orina del día que recoge el testimonio de lo sucedido por la noche debe estudiarse necesariamente por separado de otras determinaciones metabólicas30. Valores del cociente calcio:citrato superiores a 0,33 indican que la orina es potencialmente litógena, con independencia de la edad y del momento de la recogida de la orina. En un estudio previo se observó que, en niños con aparente prelitiasis, el cociente calcio:citrato correspondiente a la orina de la noche estaba incrementado en el 33,3% de las muestras y, en cambio, el mismo cociente, en la primera orina del día, estaba elevado en el 70,8% de los casos. Este era el único parámetro calculado que se relacionaba, además, con la existencia de antecedentes familiares de litiasis31. Una situación particular puede ocurrir, preferentemente, en la adolescencia, cuando la citraturia puede estar reducida y la calciuria también, con lo que la orina no será litogena, al mostrar una relación calcio:creatinina normal.
TRATAMIENTO Y PREVENCIÓN
La eliminación espontánea del cálculo, para todos los grupos de edades, sorprendentemente, rara vez sucede cuando el tamaño está por encima de los 5 mm13. El manejo de los cálculos renales en la infancia es similar al que se realiza en adultos.
Manejo del episodio agudo
El dolor debe ser abordado de forma contundente con analgésicos potentes, fundamentalmente los que inhiben la producción de PGE2, como los salicilatos y el ibuprofeno23. Pueden utilizarse, asimismo, los antiinflamatorios no esteroideos (ketorolaco) e, incluso, los analgésicos narcóticos (sulfato de morfina).
En relación con el metabolismo hídrico, si se presentan vómitos deberá garantizarse la hidratación por vía parenteral, si fuera preciso, para mantener una buena diuresis. En ausencia de fallo renal u obstrucción urinaria aguda, se aconseja mantener una infusión intravenosa 1,5 o 2 veces mayor que la necesaria para el mantenimiento de las necesidades basales.
La terapia farmacológica puede ayudar a expulsar los cálculos, mediante el uso de bloqueantes alfa adrenérgicos (tansulosin) o bloqueadores de los canales del calcio (nifedipino), que tan prometedores resultados están produciendo en adultos con cálculos localizados en el uréter distal. A este respecto, se han realizado escasos estudios en la infancia, si bien en alguno de ellos se han alcanzado resultados esperanzadores.
Es prudente filtrar la orina con el objeto de intentar recoger el cálculo y poder analizarlo.
Si existe una infección urinaria concomitante deberá ser tratada, empíricamente, tras recoger una muestra para urocultivo y solicitar el antibiograma14.
Técnicas urológicas destinadas a la rotura o la extracción de los cálculos
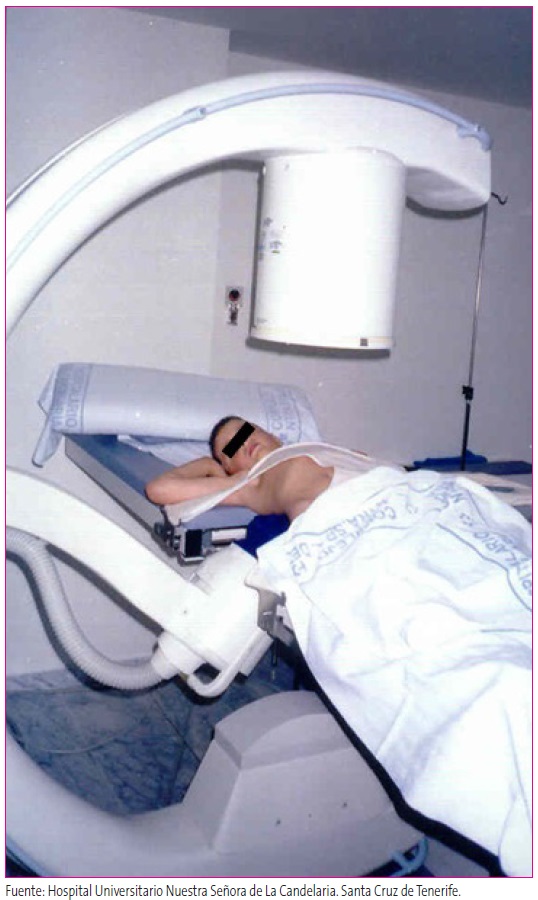
La mayoría de los cálculos renales pueden ser tratados mediante diversas técnicas. La litotricia extracorpórea (LEOC) es el procedimiento de elección para los cálculos renales y ureterales proximales menores de 1 cm (Figura 7). La nefrolitotomía percutánea (NLPC) ha demostrado una resolución satisfactoria también en los niños (grado de comprobación científica: 2, grado de recomendación: B). A veces se ha utilizado una combinación de ambas18,23. La ureteroscopia flexible (URS) también se está convirtiendo en una opción de tratamiento importante en el arsenal de la urología pediátrica para el tratamiento de los cálculos de los cálices y del polo inferior. Todos los estudios han demostrado que el uso de la endoscopia ureteral es segura en niños (grado de comprobación científica: 1; grado de recomendación: A)23.
Figura 7. Paciente diagnosticado de oxalosis prepararado para recibir una sesion de litotricia extracorpórea. Mostrar/ocultar
La cirugía abierta tiene un papel muy limitado, aunque puede ser de utilidad cuando existe la necesidad de hacer una cirugía reconstructiva adyuvante.
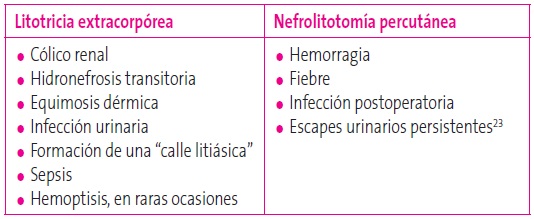
Los resultados suelen ser óptimos con las diferentes técnicas aplicadas23,32-34. El tratamiento con una sola técnica rinde un 88% de efectividad, si bien cuando se aplican las diferentes técnicas combinadas se alcanza un 97% de resolución de los diferentes casos clínicos planteados32. Se debe esterilizar la orina antes de practicar una LEOC, una URS o una NLPC. En la Tabla 5 se citan las complicaciones que pueden observarse en estas formas de tratamiento.
Tabla 5. Complicaciones del tratamiento. Mostrar/ocultar
Medidas dietéticas y farmacológicas en función de la anomalía metabólica causal
Existe mucha controversia sobre el momento en el que debe introducirse el tratamiento farmacológico. Puesto que la hipercalciuria no es una enfermedad sino una anomalía metabólica, en nuestra opinión, deben usarse los fármacos únicamente cuando se comprueban cálculos ecográficos o en los casos de hematuria macroscópica de repetición, disuria persistente, nefrocalcinosis (Figura 8) u osteopenia progresiva.
Figura 8. Nefrocalcinosis ecográfica. Se observan las pirámides renales hiperecogénicas Mostrar/ocultar
Hipercalciuria
El tratamiento inicial consiste en incrementar la ingestión de líquidos. La modificación de la alimentación forma parte imprescindible de un tratamiento eficaz. Se debe estimular el consumo de alimentos que contengan protectores de la formación de cálculos, especialmente frutas (cítricos, melón), verduras, pescados azules y cereales integrales (por su contenido en fitato). Debe recomendarse no abusar de los lácteos, de otras proteínas de origen animal y de la sal, aunque debe garantizarse un aporte de calcio compatible con las necesidades diarias del niño, por el riesgo de osteoporosis a largo plazo.
Puede realizarse un ensayo breve con una dieta con bajo contenido en calcio para determinar si el aporte exógeno de calcio contribuye a una calciuria elevada. Sin embargo, hay que tener gran precaución al tratar de restringir el aporte de calcio durante periodos prolongados (grado de comprobación científica: 3; grado de recomendación: B).
Cuando está indicado el tratamiento farmacológico, pueden utilizarse la hidroclorotiazida y otros diuréticos tiazídicos, en una dosis de 1-2 mg/kg/día2,8 (grado de comprobación científica: 3; grado de recomendación: C). El tratamiento con citrato potásico (2-4 mEq/kg/día) o citrato de potasio-magnesio también resulta útil cuando las concentraciones de citrato son bajas o si persiste la hipercalciuria a pesar de otros tratamientos (grado de comprobación científica: 4; grado de recomendación: C).
Hiperoxaluria
El tratamiento consiste en inducir una diuresis elevada. Es conveniente una restricción moderada del oxalato alimentario y un aporte regular de calcio23. La piridoxina puede ser útil para reducir las concentraciones urinarias, especialmente en la hiperoxaluria primaria (grado de comprobación científica: 4; grado de recomendación: C14,18.
Acido úrico. Hiperuricosuria
El tratamiento consiste en la alcalinización de la orina. El mantenimiento de un pH urinario entre 6 y 6,5 resulta suficiente para evitar la formación de los cálculos de ácido úrico14,18. El alopurinol a dosis de 4-10 μg/kg/día, máximo 300 μg/día, está indicado en las situaciones de hiperuricemia e hiperuricosuria. En tratamientosa largo plazo puede producirse xantinuria y favorecerse la formación de cálculos de xantina14.
Cistinuria
Es básico mantener una diuresis elevada. Una dieta baja en sal puede reducir la excreción urinaria de cistina. Es necesario emplear alcalinizantes, como citrato potásico, para mantener el pH de la orina por encima de 7. Cuando fracasa lo anterior, el uso de α-mercaptopropionil glicina o D-penicilamina puede reducir la concentración de cistina en la orina e impedir, en lo posible, la formación de cálculos. El uso de estos medicamentos puede tener efectos secundarios graves, como mielodepresión y síndrome nefrótico (grado de comprobación científica: 4; grado de recomendación: C)14,18. Los cálculos son de textura dura y más difíciles de desintegrar con litotricia extracorpórea mediante ondas de choque (LEOC).
Hipocitraturia
Las medidas dietéticas son las mismas que en el caso de la hipercalciuria. Especialmente, debe insistirse en el consumo aumentado de líquidos y frutas, y en no abusar de la sal ni de las proteínas de origen animal18. Cuando está indicado, se trata con citrato potásico en una dosis inicial de 1 mEq/kg, administrado en dos dosis divididas (grado de comprobación científica: 3; grado de recomendación: B).
Medidas dietéticas preventivas
La forma de vida en los países occidentales conlleva una serie de factores que incrementan el riesgo de litiasis. La ingesta de líquidos suele ser reducida35, se consumen alimentos hipercalóricos y con abundante sal, pero insuficientes en fibra y álcalis y, con frecuencia, se realiza poco ejercicio. Las consecuencias de todo ello son una orina deficiente en sustancias inhibidoras de la formación de cálculos y rica en sustancias favorecedoras, junto a una “epidemia” de obesidad que es factor de riesgo de la formación de cálculos28 (Anexo 1).
Anexo 1. Recomendaciones dietéticas en la hipercalciuria. Mostrar/ocultar
Por todo ello, los objetivos preventivos deberían ser los siguientes:
- Asegurar una ingesta adecuada de líquidos, sobre todo en situaciones de pérdida aguda de agua35.
- Incrementar el consumo de cítricos para incrementar el volumen de orina y su contenido en citrato.
- En cuanto a la ingesta de proteínas, se recomienda ingerir las indicadas para el rango de edad y sexo.
- Se recomienda una dieta rica en potasio. Por ello, las frutas y los vegetales deben priorizarse14.
Pese a todo esto, los síntomas recurren en el 50% de los casos, ya que entre un 10 y un 20% de los enfermos litiásicos tendrán 2-3 episodios en la vida28.
COMENTARIOS FINALES
Derivación al nefrólogo pediátrico
Básicamente, se derivarán:
- Los niños que han eliminado cálculos.
- Los que tienen hematuria macroscópica mantenida o disuria.
- Los portadores de nefrocalcinosis.
- Los diagnosticados de hipercalciuria idiopática, hacia los 12 años de edad, para la realización de una densitometría ósea23.
Pronóstico y evolución
Se ha comunicado que hasta un 24% de los pacientes recidivará de su patología2. Hasta en un 50% de los pacientes existirá repercusión sobre el riñón o las vías urinarias. Se ha descrito que la incidencia de secuelas a largo plazo puede llegar a ser de un 27,5%, siendo la asociación infección/malformación con litiasis renal la que parece tener un peor pronóstico a largo plazo y un mayor riesgo de lesión renal permanente1.
BIBLIOGRAFÍA
- 1. Camacho Díaz JA, Casas Gómez J, Amat Barnés A, Jiménez Llort A, García García L. Litiasis renal en el niño. An Esp Ped. 1996;44:225-8.
- Santos Ruiz M, Hidalgo Barquero E, García Blanco J. Urolitiasis en la infancia: revisión clínica y epidemiológica de los últimos años en nuestro medio. Vox Paediatrica. 2004;12:13-9.
- Trincheri A. Epidemiology of urolithiasis: an update. Clin Cases Miner Bon Metab. 2008;5:101-6.
- Elder SJ. Urinary Lithiasis. En: Kliegman RM, Stanton B, Geme J, Schor N, Behrman R, Kliegman RM (eds.). Nelson Textbook of Pediatrics, 19th ed. Philadelphia: Saunders; 2011.Chapter 541 [en línea] [consultado el 13/09/2014]. Disponible en: http://goo.gl/hZlkWJ
- Bush NC, Xu L, Brown BJ, Holzer MS, Gingrich A, Schuler B, et al. Hospitalizations for pediatric stone disease in United States, 2002-2007. J Urol. 2010;183:1151-6.
- Novak TE, Lakshmanan Y, Trock BJ, Gearhart JP, Matlaga BR. Sex prevalence of pediatric kidney stone disease in the United States: an epidemiologic investigation. Urology. 2009;74:104-7.
- Leusmann DB, Blaschke R, Schmandt W. Results of 5.035 stone analyses: a contribution to epidemiology of urinary stone disease. Scand J Urol Nephrol. 1990;24:205-10.
- Nicar MJ, Hill K, Pak CY. Inhibition by citrate of spontaneous precipitation of calcium oxalate in vitro. J Bone Miner Res. 1987;2:215-20.
- Meyer JL, Smith LH. Growth of calcium oxalate crystals. II. Inhibition by natural urinary crystal growth inhibitors. Invest Urol. 1975;13:36-9.
- Matlaga BR, Coe FL, Evan AP, Lingeman JE. The role of Randall's plaques in the pathogenesis of calcium stones. J Urol. 2007;177:31-8.
- Grases Freixedas F, Costa-Bauzá A. Mecanismos de la formación de los cálculos renales. En: García Nieto V, Santos Rodríguez F, Rodríguez Iturbe B (eds.). Nefrología Pediátrica, 2.ª ed. Madrid: Aula Médica; 2006. p. 917-28.
- Evan A, Lingeman J, Coe FL, Worcester E. Randall’s plaque: pathogenesis and role in calcium oxalate nephrolithiasis. Kidney Int. 2006;69:1313-8.
- Bartosh SM. Medical management of pediatric stone disease. Urol Clin North Am. 2004;31:575-87.
- Copelovitch L. Urolithiasis in children: medical approach. Pediatr Clin North Am. 2012;59:881-96.
- Areses Trapote R, Urbieta Garagorri MA, Ubetagoyena Arrieta M, Mingo Monge T, Arruebarrena Lizarraga D. Evaluación de la enfermedad renal litiásica. Estudio metabólico. An Pediatr (Barc). 2004;61:418-27.
- Defoor W, Asplin J, Jackson E, Jackson C, Reddy P, Sheldon C,et al. Results of a prospective trial to compare normal urine supersaturation in children and adults. J Urol. 2005;174:1708-10.
- Tekin A, Tekgul S, Atsu N, Sahin A, Ozen H, Bakkaloglu M. A study of the etiology of idiopathic calcium urolithiasis in children: hypocitruria is the most important risk factor. J Urol. 2000;164:162-5.
- Tekgul S, Riedmiller H, Dogan HS, Hoebeke P, Kocvara R, Nijman R, et al. Guidelines on paediatric urology. Arnhem, The Netherlands: European Association of Urology, European Society for Paediatric Urology; 2013 [en línea] [consultado el 23/09/2014]. Disponible en: http://www.guideline.gov/content.aspx?id=47872
- Campuzano S, Bousoño C, Málaga S, Díaz JJ, Rodríguez M, Campos C. Riesgo de urolitiasis en pacientes con fibrosis quística. Nefrología. 2009;29:61-6.
- Choi JN, Song JE, Shin JI, Kim HD, Kim MJ, Lee JS. Renal stone associated with the ketogenic diet in a 5-year old girl with intractable epilepsy. Yonsei Med J. 2010;51:457-9.
- García Nieto V, Dublan García K, Luís Yanes MI. ¿Los quistes renales simples son otra forma de manifestación de prelitiasis en la infancia? Nefrología. 2010;30:337-41.
- Brikowski TH, Lotan Y, Pearle MS. Climate-related increase in the prevalence of urolithiasis in the United States. Proc Natl Acad Sci USA. 2008;105:9841-6.
- Luis Yanes MI, García Nieto VM, Monge Zamorano M, Hernández González MJ. Hipercalciuria idiopática. Generalidades, diagnóstico y seguimiento en Atención Primaria. Can Pediatr. 2005;29:47-53.
- Kalia A, Travis LB, Brouhard BH. The association of idiopathic hypercalciuria and asymptomatic gross hematuria in children. J Pediatr. 1981;99:716-9.
- Polito C, La Manna A, Signoriello G, Marte A. Recurrent abdominal pain in childhood urolithiasis. Pediatrics. 2009;124:e1088-94.
- Roy S 3rd, Stapleton FB, Noe HN, Jerkins GJ. Hematuria preceding renal calculus formation in children with hypercalciuria. Pediatr. 1981;99:712-5.
- Moore ES. Hypercalciuria in children. Contr Nephrol. 1981;27:20-32.
- Straub M, Strohmaier WL, Berg W, Beck B, Hoppe B, Laube N, et al. Diagnosis and metaphylaxis of stone disease. Consensus concept of the National Working Committee on Stone Disease for the upcoming German Urolithiasis Guideline. World J Urol. 2005;23:309-23.
- Montañés Bermúdez R, Gràcia Garcia S, Fraga Rodríguez GM, Escribano Subías J, Díez de los Ríos Carrasco MJ, Alonso Melgar A, et al. Documento de consenso: recomendaciones sobre la utilización de ecuaciones para la estimación del filtrado glomerular en niños. An Pediatr (Barc). 2013;80:326.e1-326.e13
- García-Nieto V, Luis-Yanes MI. El nefrólogo y la litiasis renal, ¿la toma o la deja? Nefrología. 2013;33:155-9.
- Luis-Yanes MI, Monge-Zamorano M, Hernández-González MJ, Fraga-Bilbao F, González-Cerrato S, García-Nieto V. Determination in two moments of the day of two lithogenic risk factors in the urine of children with prelithiasis. Pediatr Nephrol. 2012;27:1713.
- Cabezalí Barbancho D, Gómez Fraile A, Tejedor Sánchez R, López Díaz M, Romero Otero J, López Vázquez F, et al. Nuestra experiencia en el manejo endourológico de las litiasis en el tracto urinario en la infancia. Cir Pediatr. 2008;21:15-8.
- Resorlu B, Unsal A, Tepeler A, Atis G, Tokatli Z, Oztuna D, et al.Comparison of retrograde intrarenal surgery and mini-percutaneous nephrolithotomy in children with moderate-size kidney stones: results of multi-institutional analysis.Urology. 2012;80:519-23.
- Srisubat A, Potisat S, Lojanapiwat B, Setthawong V, Laopaiboon M. Extracorporeal shock wave lithotripsy (ESWL) versus percutaneous nephrolithotomy (PCNL) or retrograde intrarenal surgery (RIRS) for kidney stones. Cochrane Database Syst Rev. 2009;(4):CD007044.
- Sáez-Torres C, Grases F, Rodrigo D, García-Raja AM, Gómez C, Frontera G. Risk factors for urinary stones in healthy schoolchildren with and without a family history of nephrolithiasis. Pediatr Nephrol. 2013;28:639-45.
LECTURAS RECOMENDADAS
-
Brikowski TH, Lotan Y, Pearle MS. Climate-related increase in the prevalence of urolithiasis in the United States. Proc Natl Acad Sci USA. 2008;105:9841-6.
Una publicación imprescindible.Disponible en: http://www.pnas.org/content/105/28/9841.full
-
Copelovitch L. Urolithiasis in Children. Medical Approach. Pediatr Clin North Am. 2012;59(4):881-96.
Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3426770/
-
De Pablo Galán L. La mineralogía de los cálculos renales, un caso de mineralogía patológica humana. Un. Nac. Autón. México. Inst. Geología. Revista. 1988;7(2):226-31.
Bonita, interesante y curiosa publicación sobre cálculos.
-
Tekgul S, Riedmiller H, Dogan HS, Hoebeke P, Kocvara R, Nijman R, et al. Guidelines on paediatric urology. Arnhem, The Netherlands: European Association of Urology, European Society for Paediatric Urology; 2013.
Disponible en: http://www.guideline.gov/content.aspx?id=47872